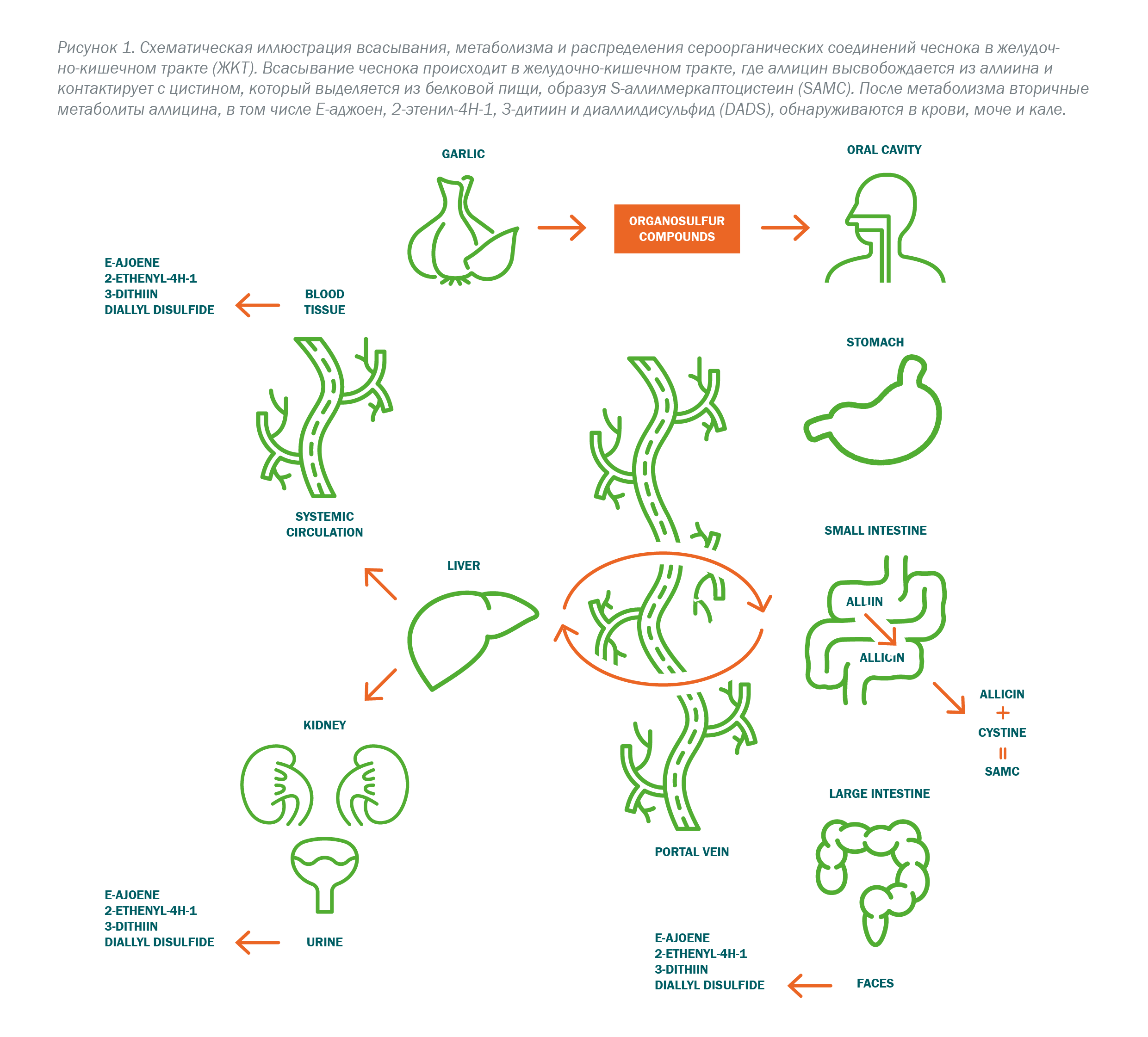
Дата публикации: 20 дек 2025Краткий обзор потенциальной пользы чеснока для здоровья человека на основании результатов клинических исследований
Краткое изложениеЧеснок — это полифенольная и сераорганическая приправа, употребляемая с давних времён. Как показывают несколько in vitro и in vivo клинических исследований, чеснок и его вторичные метаболиты обладают антиоксидантным, противовоспалительным и липидоснижающим свойством, благодаря чему оказывают лечебно-профилактическое действие при таких заболеваниях, как рак, сердечно-сосудистые расстройства и нарушение обмена веществ, артериальное давление, а также диабет. Цель настоящего обзора - предоставить наиболее подробный обзор воздействия приема и приготовления чеснока, экстракта чеснока и биологически-активных компонентов, полученных из чеснока, на оксидативный стресс, воспаление, рак, сердечно-сосудистые расстройства и расстройства обмена веществ, заболевания кожи и костей и прочие часто встречающиеся заболевания. В 83 рассмотренных исследованиях на людях сообщалось, что употребление чеснока изменяет многочисленные биомаркеры различных заболеваний; а совместный прием чеснока с лекарственными средствами или прочими пищевыми матрицами является безопасным и пролонгирует лечебное воздействие. Также обсуждается быстрый метаболизм и плохая биодоступность, которые ограничивают терапевтическое использование чеснока в последнее время.
Ключевые словаЧеснок, содержащие серу компоненты, благоприятное воздействие на здоровье полифенолов, метаболизм и биодоступность.
ВведениеСпеции используются не только для усиления аромата, вкуса и цвета еды, но также применяются с терапевтическими целями из-за их потенциальной способности предотвращать различные острые и хронические заболевания. Различные биоактивные составляющие специй, включающие алкалоиды, таннины, витамины и фенольные дитерпены, флавоноиды и полифенолы, а также серосодержащие вещества, обладают различными терапевтическими свойствами, благодаря своим антиоксидантым, антиканцерогенным, противоопухолевым, противовоспалительным и снижающим холестерин и глюкозу свойствам.[1]
Чеснок (Allium sativum L.) – относится к семейству Амариллисовые; выращивается во всем мире и обладает значимыми лечебными свойствами. В 1550 г. до нашей эры антибиотики и фармацевтическая продукция не были доступны, поэтому чеснок использовался для медицинских целей во время различных эпидемий, таких как тиф, дизентерия, холера, и грипп [2]. Терапевтическое действие чеснока в основном обусловлено впечатляющей активностью его биоактивных компонентов, таких как органические сульфиды [3], сапонины [4], фенольные составляющие [5] и полисахариды [6]. Например, различные исследования in vitro и in vivo показали, что составляющие чеснока способны изменять сигнальные пути, включая ядерный фактор-kB и место интеграции Wingless [7], матриксные металлопротеиназы, клеточный фактор эритроид 2-подобный 2, протеинкиназа B (pAkt), активируемая митогеном протеинкиназа, c-Jun N-терминальная киназа, каспазы, р38,
Трансформирующий фактор роста бета 1 (TGF-β1), TGF-β тип II рецептор, psmad 2/3, smad4 и smad [8,9], цитокины, молекулы межклеточной адгезии [10], рецептор-зависимый латентный фактор транскрипции, локализованный в клеточной цитоплазме [11], 5'АМФ-активируемая протеинкиназа [12], васкулоэндотелиальный фактор роста [13], циклооксигеназа-2, индуцибельная синтаза оксида азота, Akt/mTor [14] и Keap1 [15], что в свою очередь ведет к повышению противовоспалительных и антиоксидантных свойств, а так же оказывает химиопрофилактическое, антипролиферативное, анти-ангиогенное, противодиабетическое и кардиопротективное действие. Однако, следует иметь ввиду, что указанные составляющие обладают низкой доступностью. Например, в рандомизированном контролируемом исследовании описано, что после перорального приема от 1 до 3 г порошка чеснока сухого, в моче через 6 и 24 часа не были обнаружены сераорганических соединений диаллилдисульфида (DADS) и диаллилсульфида (DAS) ]16]. Кроме того, аллилтиосульфаты, содержащиеся в препарате чеснока, подвергаются активному метаболизму с образованием аллилметилсульфида, который в основном присутствует в дыхании [17].
Таким образом, цель настоящей работы – предоставить комплексный обзор клинических исследований за прошедшие 20 лет, описывающих терапевтическое действие чеснока при различных заболеваниях у людей: рак, сердечно-сосудистые патологии, диабет, нарушение обмена веществ, остеопороз и заболевания кожи, с акцентом на его антиоксидантных, противовоспалительных и липидоснижающих свойствах. В настоящем обзоре представлены основные молекулярные механизмы чеснока, обеспечивающие его многообещающее положительное воздействие на здоровье после приема.
Чеснок (Allium sativum L.) – относится к семейству Амариллисовые; выращивается во всем мире и обладает значимыми лечебными свойствами. В 1550 г. до нашей эры антибиотики и фармацевтическая продукция не были доступны, поэтому чеснок использовался для медицинских целей во время различных эпидемий, таких как тиф, дизентерия, холера, и грипп [2]. Терапевтическое действие чеснока в основном обусловлено впечатляющей активностью его биоактивных компонентов, таких как органические сульфиды [3], сапонины [4], фенольные составляющие [5] и полисахариды [6]. Например, различные исследования in vitro и in vivo показали, что составляющие чеснока способны изменять сигнальные пути, включая ядерный фактор-kB и место интеграции Wingless [7], матриксные металлопротеиназы, клеточный фактор эритроид 2-подобный 2, протеинкиназа B (pAkt), активируемая митогеном протеинкиназа, c-Jun N-терминальная киназа, каспазы, р38,
Трансформирующий фактор роста бета 1 (TGF-β1), TGF-β тип II рецептор, psmad 2/3, smad4 и smad [8,9], цитокины, молекулы межклеточной адгезии [10], рецептор-зависимый латентный фактор транскрипции, локализованный в клеточной цитоплазме [11], 5'АМФ-активируемая протеинкиназа [12], васкулоэндотелиальный фактор роста [13], циклооксигеназа-2, индуцибельная синтаза оксида азота, Akt/mTor [14] и Keap1 [15], что в свою очередь ведет к повышению противовоспалительных и антиоксидантных свойств, а так же оказывает химиопрофилактическое, антипролиферативное, анти-ангиогенное, противодиабетическое и кардиопротективное действие. Однако, следует иметь ввиду, что указанные составляющие обладают низкой доступностью. Например, в рандомизированном контролируемом исследовании описано, что после перорального приема от 1 до 3 г порошка чеснока сухого, в моче через 6 и 24 часа не были обнаружены сераорганических соединений диаллилдисульфида (DADS) и диаллилсульфида (DAS) ]16]. Кроме того, аллилтиосульфаты, содержащиеся в препарате чеснока, подвергаются активному метаболизму с образованием аллилметилсульфида, который в основном присутствует в дыхании [17].
Таким образом, цель настоящей работы – предоставить комплексный обзор клинических исследований за прошедшие 20 лет, описывающих терапевтическое действие чеснока при различных заболеваниях у людей: рак, сердечно-сосудистые патологии, диабет, нарушение обмена веществ, остеопороз и заболевания кожи, с акцентом на его антиоксидантных, противовоспалительных и липидоснижающих свойствах. В настоящем обзоре представлены основные молекулярные механизмы чеснока, обеспечивающие его многообещающее положительное воздействие на здоровье после приема.
Поиск литературыБыл проведён всесторонний поиск с использованием электронных баз данных, включая Medline, Scopus, Google Scholar и Web of Science, а также были рассмотрены соответствующие клинические испытания, касающиеся воздействия чеснока на заболевания человека. Ключевые слова “чеснок”, “эффекты чеснока”, “биологически активные соединения чеснока”, “полифенолы чеснока”, “аллицин”, “аллиин”, “аллилпропилдисульфид”, “диаллил трисульфид (DATS)”, “аджоен”, “S-аллилцистеин”, “S-аллилмеркаптоцистеин” (SAMC), “винилдитиины”, “выдержанный чеснок”, “зубчики чеснока”., “метаболизм чеснока”, ”всасывание чеснока“, ”биодоступность чеснока“, ”антиоксидантная способность чеснока“, ” противовоспалительные свойства чеснока“, ”гиполипидемический эффект чеснока“, а так же была искали связь чеснока с каждым конкретным заболеванием (например, ”чеснок и рак“, "чеснок и рак толстой кишки”, “чеснок и рак предстательной железы”, “чеснок и рак пищевода”, “чеснок и рак гортани” и т.д.). Все изученные статьи были опубликованы в период с 2000 по 2020 год.
Биологически активные соединения чеснока Чеснок считается эффективной специей благодаря многочисленным питательным компонентам, фитохимическим веществам и клетчатки, входящих в его состав. Он содержит большое количество калия, фосфора, цинка и серы, умеренное количество селена, кальция, магния, марганца, железа и маленькое количество натрия, витаминов А и С и комплекса витаминов группы В [18]. В последние годы значительное внимание уделялось его основным биологически активным соединениям, в частности полифенолам, флавоноидам, флаванолам, дубильным веществам [5,19], сапонинам [4], полисахаридам [6], серосодержащим соединениям (включая аллиин, аллицин, аджоен, аллилпропилдисульфид, DAT, S-аллилцистеин, винилдитиины, SAMC), энзимам (такие как аллиназа, пероксидаза, мирозиназа) и другим соединениям, таким как β-фелландрен, фелландрен, цитраль, линалоол и гераниол [3]. В чесноке содержится более двадцати хорошо известных полифенольных соединений, включая кемпферол-3,7-ди-О-рамнозид, кемпферол-3 глюкуронид, кемпферол-3-О-глюкозид, кемпферол-3-О-бета-D-глюкозид-7-О-альфа-l-рамнозид, лютеолин и апигенин [20]. Кроме того, он содержит 17 аминокислот, в том числе восемь основных аминокислот [21]. Как правило, биологически активные соединения присутствуют в цельном чесноке, но после измельчения или раздавливания, после различных типов химических реакций было обнаружено большее количество соединений, таких как аллицин, DAS, DADS, дитиины и аджоен [22,23].
Клинические испытания чеснока В последнее время употребление чеснока привлекает особое внимание вследствие терапевтического действия против рака, сердечных заболеваний, артериального давления, диабета, заболеваний костей и кожи, а также других патологий, благодаря его антиоксидантному, противовоспалительному и гиполипидемическому действию. Все клинические исследования представлены в таблицах 1-4.
Свойства чеснокаАнтиоксидантная способностьЧеснок обладает сильными антиоксидантными свойствами благодаря содержащимся в нем питательным веществам и фенольным соединениям [31]. Например, антиоксидантные свойства выдержанного экстракта чеснока (AGE) уменьшают количество активных форм кислорода, которые образуются в результате повышенного метаболизма или хронического воспаления, предотвращая, таким образом, эндотелиальную дисфункцию - ранний маркер атеросклероза [32].
В ходе рандомизированного двойного слепого плацебо-контролируемого диетологического исследования потребление экстракта чеснока (GE) в дозе 400 мг/день в течение трех месяцев улучшало антиоксидантный статус, снижая, в свою очередь, риск сердечно-сосудистых заболеваний у пациентов с ожирением за счет модулирования эндотелиальных биомаркеров, таких как С-реактивный белок (hs-CRP), липопротеины низкой плотности (ЛПНП), уровень холестерина, липопротеины высокой плотности (ЛПВП), триглицериды (ТГ) и ингибитор активатора плазминогена 1 (PAI-1) [33]. Кроме того, у пациентов с сахарным диабетом после 30 дней приёма 3,6 г зубчика чеснока в день повышается активность антиоксидантов, таких как супероксиддисмутаза (SOD), каталаза (CAT) и активность глутатионпероксидазы (GPx) в циркулирующих эритроцитах человека по сравнению с контролем [34]. Недавний мета-анализ клинических исследований показал, что добавки с чесноком модулируют маркеры окислительного стресса, включая общую антиоксидантную способность и малондиальдегид (MDA) [35]; например, таблетка чеснока (Garlet) оказывала значительное влияние на окислительный стресс, снижая уровень MDA и повышая концентрацию TAC у женщин с остеопорозом в постменопаузе в дозе 1200 мкг аллицина ежедневно в течение одного месяца по сравнению с плацебо [36]. Кроме того, приём чеснока синергически улучшал (устойчивость и выносливость) тренировочный эффект против окислительного стресса за счёт модулирования маркеров окислительного стресса, таких как TAC и MDA, после восьми недель приема чесночной капсулы в дозировке 250 мг в день в течение восьми недель [37]. Однако, другое двойное слепое перекрёстное пилотное исследование, проведённое на пациентах с сахарным диабетом 2 типа, показало, что AGE при приёме 1200 мг в день в течение 4 недель не оказывает существенного влияния на окислительный стресс в эндотелиальной ткани [38]. Аналогичные результаты были получены в рандомизированном перекрёстном исследовании, в котором у мужчин с ишемической болезнью сердца приём добавки AGE в дозе 2,4 г в день в течение двух недель существенно не изменял маркеры окислительного стресса и системного воспаления в ходе исследования, даже если обнаруживалось улучшение эндотелийзависимой дилатации по сравнению с исходным уровнем и улучшение функции эндотелия [39].
Наконец, несколько перекрёстных исследований показали, что употребление в пищу продуктов с высоким содержанием антиоксидантных специй, включая чеснок, улучшает антиоксидантный статус у онкологических больных и постпрандиальную липемию у здоровых взрослых с избыточным весом по сравнению с приёмом пищи с низким содержанием специй [40,41]. Кроме того, потребление 400 мг чеснока и 1 мг аллицина в день через девять недель снижало окислительный стресс у беременных женщин, подверженных риску развития преэклампсии, но не оказал существенного влияния на общую окислительную способность и на течение беременности [42]. Противовоспалительные свойства Различные хронические заболевания, такие как рак и сердечно-сосудистые заболевания, связаны с воспалительными процессами; для их профилактики используются различные виды терапевтических и природных средств [43]. В этом контексте было показано, что чеснок оказывает мощное противовоспалительное действие, снижая уровень биомаркеров воспаления у пациентов с терминальной стадией почечной недостаточности у взрослых пациентов. Двойное слепое рандомизированное клиническое исследование показало значительное снижение уровня воспалительных цитокинов, таких как интерлейкин 6 (IL-6), С-реактивный белок (CRP) и скорость оседания эритроцитов, при введении стандартизированного экстракта чеснока GE по 400 мг два раза в день в течение восьми недель пациентам, находящимся на перитонеальном диализе [44,45]. Кроме того, мета-анализ показал, что добавки с чесноком, включая AGE, чесночный порошок и чесночные капсулы, снижали концентрацию фактора некроза опухоли альфа (TNF-α) и СРБ в сыворотке крови, но не влияли на уровень адипонектина и лептина в сыворотке у здоровых взрослых [46].
Иммунные клетки отвечают за противовоспалительный эффект; выдержанный чеснок содержит различные соединения, которые могут улучшить работу иммунной системы, модулируя выработку цитокинов. Например, потребление добавок с выдержанным чесноком в дозе 2,56 г в день в течение 90 дней повышало активность иммунных клеток, таких как γδ и естественные киллеры (NK), и уменьшало воспаление за счёт снижения уровня TNF-α - и IL-6 у взрослых с ожирением [47]. Интересно, что та же доза GE повышала функцию иммунных клеток, уменьшая тяжесть кашля и гриппа [48] и увеличивая экскрецию цитокина IL-12 с мочой, даже если не было обнаружено существенного влияния на IL-8 и TNF-α [16]. Кроме того, в рандомизированном двойном слепом плацебо-контролируемом клиническом исследовании была обнаружена отрицательная корреляция между сераорганическими соединениями выдержанного экстракта чеснока (AGE) и воспалением, вызванным ожирением. После приёма добавки AGE в дозе 3,6 г в день в течение шести недель S-аллилцистеин (SAC) уменьшал воспаление, вызванное ожирением, за счёт высвобождения сероводорода (H2S) увеличивая его эндогенных продукты [49]. Кроме того, добавки с чесноком увеличивали микробное разнообразие, а также улучшали состояние при воспалении у пациентов с неконтролируемой гипертонией [50], в то время как потребление чеснока в дозировке 2,1 г в день в течение 12 недель не оказывало существенного влияния на воспаление у лиц с избыточным весом [51] и у пациентов с сахарным диабетом 2 типа с высоким риском развития сердечно-сосудистых заболеваний [38]. Гиполипидемический эффектЧеснок продемонстрировал многообещающий гиполипидемический эффект у пациентов с гиперлипидемией за счёт снижения концентрации холестерина в сыворотке крови [52]. У больных сахарным диабетом сочетание чеснока с оливковым маслом эффективно регулировало уровень холестерина и триглицеридов в сыворотке крови, а также дислипидемию [53]. Силаги и Нил (Silagy and Neil, 1994) предположили, что чеснок в непорошковой и порошкообразной формах, несомненно, снижает уровень липидов в сыворотке крови в течение одного-трех месяцев. Через четыре месяца потребления GE повысился уровень ЛПВП и снизился уровень ЛПНП и холестерина у 23 пациентов с гиперлипидемией [54]. Несколько исследований показали, что приём выдержанного черного чеснока или чесночных таблеток в дозе 300 мг или 6 г два раза в день в течение 4 или 12 недель снижал уровни общего холестерина (ОХ), триглицеридов и ЛПНП, и повышал уровень ЛПВП у пациентов с умеренной гиперхолестеринемией и дислипидемией или у пациентов с диабетом 2-го типа [55-57]. Кроме того, выдержанный чеснок в дозе 2,4 г в день в течение двух недель снижал уровень холестерина и ТГ у пациентов с ишемической болезнью сердца [39]. В другом рандомизированном двойном слепом плацебо-контролируемом исследовании таблетка чесночного порошка в дозе 10,8 мг в день в течение 12 недель снижала концентрацию триацилглицерина у здоровых добровольцев [58]. Кроме того, приём кишечнорастворимой таблетки чесночного порошка, содержащая 400 мг чеснока и аллицина в дозе 1 мг два раза в день снижал уровень холестерина и ЛПНП, что было продемонстрировано в ходе простого слепого исследования с участием 150 пациентов с гиперхолестеринемией [59].
В ходе рандомизированного двойного слепого плацебо-контролируемого диетологического исследования потребление экстракта чеснока (GE) в дозе 400 мг/день в течение трех месяцев улучшало антиоксидантный статус, снижая, в свою очередь, риск сердечно-сосудистых заболеваний у пациентов с ожирением за счет модулирования эндотелиальных биомаркеров, таких как С-реактивный белок (hs-CRP), липопротеины низкой плотности (ЛПНП), уровень холестерина, липопротеины высокой плотности (ЛПВП), триглицериды (ТГ) и ингибитор активатора плазминогена 1 (PAI-1) [33]. Кроме того, у пациентов с сахарным диабетом после 30 дней приёма 3,6 г зубчика чеснока в день повышается активность антиоксидантов, таких как супероксиддисмутаза (SOD), каталаза (CAT) и активность глутатионпероксидазы (GPx) в циркулирующих эритроцитах человека по сравнению с контролем [34]. Недавний мета-анализ клинических исследований показал, что добавки с чесноком модулируют маркеры окислительного стресса, включая общую антиоксидантную способность и малондиальдегид (MDA) [35]; например, таблетка чеснока (Garlet) оказывала значительное влияние на окислительный стресс, снижая уровень MDA и повышая концентрацию TAC у женщин с остеопорозом в постменопаузе в дозе 1200 мкг аллицина ежедневно в течение одного месяца по сравнению с плацебо [36]. Кроме того, приём чеснока синергически улучшал (устойчивость и выносливость) тренировочный эффект против окислительного стресса за счёт модулирования маркеров окислительного стресса, таких как TAC и MDA, после восьми недель приема чесночной капсулы в дозировке 250 мг в день в течение восьми недель [37]. Однако, другое двойное слепое перекрёстное пилотное исследование, проведённое на пациентах с сахарным диабетом 2 типа, показало, что AGE при приёме 1200 мг в день в течение 4 недель не оказывает существенного влияния на окислительный стресс в эндотелиальной ткани [38]. Аналогичные результаты были получены в рандомизированном перекрёстном исследовании, в котором у мужчин с ишемической болезнью сердца приём добавки AGE в дозе 2,4 г в день в течение двух недель существенно не изменял маркеры окислительного стресса и системного воспаления в ходе исследования, даже если обнаруживалось улучшение эндотелийзависимой дилатации по сравнению с исходным уровнем и улучшение функции эндотелия [39].
Наконец, несколько перекрёстных исследований показали, что употребление в пищу продуктов с высоким содержанием антиоксидантных специй, включая чеснок, улучшает антиоксидантный статус у онкологических больных и постпрандиальную липемию у здоровых взрослых с избыточным весом по сравнению с приёмом пищи с низким содержанием специй [40,41]. Кроме того, потребление 400 мг чеснока и 1 мг аллицина в день через девять недель снижало окислительный стресс у беременных женщин, подверженных риску развития преэклампсии, но не оказал существенного влияния на общую окислительную способность и на течение беременности [42]. Противовоспалительные свойства Различные хронические заболевания, такие как рак и сердечно-сосудистые заболевания, связаны с воспалительными процессами; для их профилактики используются различные виды терапевтических и природных средств [43]. В этом контексте было показано, что чеснок оказывает мощное противовоспалительное действие, снижая уровень биомаркеров воспаления у пациентов с терминальной стадией почечной недостаточности у взрослых пациентов. Двойное слепое рандомизированное клиническое исследование показало значительное снижение уровня воспалительных цитокинов, таких как интерлейкин 6 (IL-6), С-реактивный белок (CRP) и скорость оседания эритроцитов, при введении стандартизированного экстракта чеснока GE по 400 мг два раза в день в течение восьми недель пациентам, находящимся на перитонеальном диализе [44,45]. Кроме того, мета-анализ показал, что добавки с чесноком, включая AGE, чесночный порошок и чесночные капсулы, снижали концентрацию фактора некроза опухоли альфа (TNF-α) и СРБ в сыворотке крови, но не влияли на уровень адипонектина и лептина в сыворотке у здоровых взрослых [46].
Иммунные клетки отвечают за противовоспалительный эффект; выдержанный чеснок содержит различные соединения, которые могут улучшить работу иммунной системы, модулируя выработку цитокинов. Например, потребление добавок с выдержанным чесноком в дозе 2,56 г в день в течение 90 дней повышало активность иммунных клеток, таких как γδ и естественные киллеры (NK), и уменьшало воспаление за счёт снижения уровня TNF-α - и IL-6 у взрослых с ожирением [47]. Интересно, что та же доза GE повышала функцию иммунных клеток, уменьшая тяжесть кашля и гриппа [48] и увеличивая экскрецию цитокина IL-12 с мочой, даже если не было обнаружено существенного влияния на IL-8 и TNF-α [16]. Кроме того, в рандомизированном двойном слепом плацебо-контролируемом клиническом исследовании была обнаружена отрицательная корреляция между сераорганическими соединениями выдержанного экстракта чеснока (AGE) и воспалением, вызванным ожирением. После приёма добавки AGE в дозе 3,6 г в день в течение шести недель S-аллилцистеин (SAC) уменьшал воспаление, вызванное ожирением, за счёт высвобождения сероводорода (H2S) увеличивая его эндогенных продукты [49]. Кроме того, добавки с чесноком увеличивали микробное разнообразие, а также улучшали состояние при воспалении у пациентов с неконтролируемой гипертонией [50], в то время как потребление чеснока в дозировке 2,1 г в день в течение 12 недель не оказывало существенного влияния на воспаление у лиц с избыточным весом [51] и у пациентов с сахарным диабетом 2 типа с высоким риском развития сердечно-сосудистых заболеваний [38]. Гиполипидемический эффектЧеснок продемонстрировал многообещающий гиполипидемический эффект у пациентов с гиперлипидемией за счёт снижения концентрации холестерина в сыворотке крови [52]. У больных сахарным диабетом сочетание чеснока с оливковым маслом эффективно регулировало уровень холестерина и триглицеридов в сыворотке крови, а также дислипидемию [53]. Силаги и Нил (Silagy and Neil, 1994) предположили, что чеснок в непорошковой и порошкообразной формах, несомненно, снижает уровень липидов в сыворотке крови в течение одного-трех месяцев. Через четыре месяца потребления GE повысился уровень ЛПВП и снизился уровень ЛПНП и холестерина у 23 пациентов с гиперлипидемией [54]. Несколько исследований показали, что приём выдержанного черного чеснока или чесночных таблеток в дозе 300 мг или 6 г два раза в день в течение 4 или 12 недель снижал уровни общего холестерина (ОХ), триглицеридов и ЛПНП, и повышал уровень ЛПВП у пациентов с умеренной гиперхолестеринемией и дислипидемией или у пациентов с диабетом 2-го типа [55-57]. Кроме того, выдержанный чеснок в дозе 2,4 г в день в течение двух недель снижал уровень холестерина и ТГ у пациентов с ишемической болезнью сердца [39]. В другом рандомизированном двойном слепом плацебо-контролируемом исследовании таблетка чесночного порошка в дозе 10,8 мг в день в течение 12 недель снижала концентрацию триацилглицерина у здоровых добровольцев [58]. Кроме того, приём кишечнорастворимой таблетки чесночного порошка, содержащая 400 мг чеснока и аллицина в дозе 1 мг два раза в день снижал уровень холестерина и ЛПНП, что было продемонстрировано в ходе простого слепого исследования с участием 150 пациентов с гиперхолестеринемией [59].
Терапевтические эффекты чеснока при распространённых заболеваниях у людейРакРак является одной из основных причин смертности во всем мире. Согласно Национальной онкологической базе данных, а также данным программы по течению, распространённости и исходам злокачественных новообразований, в 2019 году рак был выявлен у 16,9 миллиона человек, и это число, вероятно, возрастёт до более чем 22,1 миллиона к 2030 году [60]. Научно обоснованная система оценки здоровья, разработанная Управлением по лекарственным средствам, не выявила достоверных доказательств связи между чесноком и снижением риска развития рака желудка, молочной железы и легких [61]. Однако сообщается о достоверных доказательствах корреляции употребления чеснока и снижения риска развития рака толстой кишки, предстательной железы, пищевода, гортани, полости рта, яичников и почечно-клеточного рака; но все эти исследования были наблюдательными, количество таких исследований, которые в данном анализе считаются научно обоснованными, сильно мало, и число участников, как правило, невелико. В результате связь между чесноком и снижением риска развития рака все ещё остаётся неопределённой [62,63]. Интересно, что чеснок может облегчить симптомы различных раковых заболеваний, включая рак молочной железы, толстой кишки, желудка, лёгких и поджелудочной железы. Это может быть терапевтическим потенциалом для специфического лечения рака, о котором сообщалось в клинических исследованиях на людях, представленных и обсуждаемых в таблице 2. В этом контексте индивидуально подобранные диеты с дополнительными функциональными элементами, включая функциональные фитохимические вещества, такие как соединения аллиловой серы или аллицин, способствуют выработки большого количества антиоксидантов для пациентов, проходящих химиотерапию и находящихся в стадии ремиссии [40]. Рандомизированное контролируемое исследование с участием выживших после рака молочной в течение шести месяцев показало, что приверженность к средиземноморской диете увеличивало потребление противовоспалительных специй, таких как чеснок [63]. Ещё одно рандомизированное двойное слепое факториальное исследование чеснока выявило снижение частоты возникновения предраковых поражений желудка или рака желудка [64], в то время как потребление 200 мг синтетического аллитрида (диаллилтрисульфида) со 100 мг селена снижало риск развития рака желудка [65]; аналогичные результаты были получены при приёме чеснока в дозе 200 мг в течение 7,3 лет. Приём капсул или чесночного масла, дистиллированного паром, по 1 мг два раза в день уменьшал прогрессирующие поражения желудка [64]. Кроме того, при длительном употреблении чеснока, чесночных добавок или чеснока в виде витаминов снижаются риск развития рака желудка [66], предраковых поражений желудка [67] и смертности [68]. Приём чеснока в дозе по две капсулы два раза в день в течение 7,3 лет повышал содержание фолиевой кислоты в сыворотке крови и устранял умеренный дефицит фолиевой кислоты у пациентов с поражениями желудка в сельской местности Китая [69]. Кроме того, потребление чесночных добавок весом от 0,60 до 3,65 кг в год в течение двух лет было значительно связано со снижением риска развития колоректальной аденомы, которая является предвестником колоректального рака (КРР) [70,71]. Эпидемиологический обзор рандомизированных контролируемых исследований показал, что применение GE уменьшает количество аденом толстого кишечника и колоректального рака у пациентов с КРР [72] за счёт увеличения активности NK-клеток [73]. Соответственно, прием AGE в дозе четыре капсулы в день в течение шести месяцев предотвращал снижение количества NK-клеток у пациентов с раком печени и поджелудочной железы [73].
Несколько эпидемиологических исследований, проведённых среди населения Китая, выявили значительную обратную зависимость между потреблением сырого чеснока или его компонентов - 8,4 г или 33,4 г в неделю в течение семи лет и раком лёгких [74]. Наконец, экстракт чеснока GE продемонстрировал профилактический эффект в отношении фебрильной нейропатии после получения химиотерапии у пациентов с гематологическими злокачественными новообразованиями, потенциально снижая риск связанной с химиотерапией фебрильной нейтропении после приёма GE в дозе 900 мг в день в течение трех недель по сравнению с плацебо [75].
В качестве объяснений химиопрофилактических эффектов чеснока используются многочисленные механизмы, включая ингибирование образования аддуктов ДНК, ингибирование мутагенеза путём блокирования метаболизма, посредством удаления свободных радикалов или путём уменьшения пролиферации клеток и роста опухолей [74]. В этом контексте Чаррон и соавт. [76] провели клиническое исследование экспрессии генов, связанных с иммунитетом, апоптозом и метаболизмом ксенобиотиков у людей, после ежедневного употребления 5 г сырого измельчённого чеснока в течение 10 дней. Однократный приём пищи, содержащий сырой измельчённый чеснок, активизировал экспрессию семи генов, таких как активирующий белок с мотивом активации иммунорецептора на основе тирозина 1, ядерный транслокатор арилуглеводородного рецептора, арилуглеводородный рецептор, индуцируемый гипоксией фактор 1α, c-Jun, ядерный фактор активированные Т-клетки, онкостатин M и гомолог вируса ретикулоэндотелиоза птиц V-rel в крови здоровых добровольцев, таким образом, подавляя онкогенез. Сердечно-сосудистые заболеванияВ настоящее время сердечно-сосудистые заболевания (ССЗ) являются основной причиной заболеваемости и смертности -во всем мире ежегодно умирает 17,3 миллиона человек, и ожидается, что к 2030 году это число превысит 23,6 миллиона [77]. Многие факторы риска влияют на развитие сердечно-сосудистых заболеваний, включая сахарный диабет 2 типа, ожирение, резистентность к инсулину, высокое артериальное давление, метаболический синдром, высокий уровень триглицеридов в сыворотке крови и липидный профиль плазмы [78]. Согласно современным исследованиям, чеснок, благодаря синергическому действию его питательных и фитохимических компонентов, может значительно снизить риск развития атеросклероза, гипертонии, диабета, гиперлипидемии, инфаркта миокарда и ишемического инсульта [79]. Например, атеросклероз и воспаление сосудов обычно сопровождаются окислительным стрессом, дисфункцией эндотелия и выработкой воспалительных цитокинов [80,81]. С точки зрения диетического подхода чеснок играет потенциальную роль в профилактике и лечении атеросклероза и инфаркта миокарда [82,83], что было продемонстрировано в рандомизированном исследовании, проведённом с использованием выдержанного экстракта чеснока AGE и суррогата жировой ткани при прогрессирующем коронарном атеросклерозе. В исследовании сообщалось об уменьшении роста коронарного атеросклероза при приеме 250 мг AGE ежедневно в течение 12 месяцев за счёт уменьшения эпикардиальной жировой ткани, перикардиальной жировой ткани, периаортальной жировой ткани и подкожной жировой ткани [84]. Кроме того, AGE предотвращал процесс развития атеросклероза, улучшая микроциркуляцию у пациентов в дозе 2400 мг AGE в сутки [85]. Более того, растительный препарат чеснока, богатый изофлавоноидами, в 1,5 раза замедлял прогрессирование атеросклероза у женщин в постменопаузе в дозе 500 мг в течение 12 месяцев после приема [86]. Другое рандомизированное двойное слепое исследование продемонстрировало, что приём 2400 мг AGE в день в течение 52 недель уменьшал количество бляшек в коронарных артериях у пациентов с метаболическим синдромом [87], но существенного влияния на уровень липопротеидов выявлено не было [88]. С другой стороны, приём AGE в дозе 6 г ежедневно в течение 12 недель снижал уровень липопротеина В и повышал уровень ЛПВП, демонстрируя кардиопротекторный эффект у пациентов с умеренной гиперхолестеринемией [55]. Кроме того, GE, принимаемый в дозе 400 мг в день в течение трех месяцев, изменял маркеры функции эндотелия, такие как hs-CRP, PAI-1, холестерин (общий, ЛПНП, ЛПВП) и триглицериды, а также подавлял хроническое воспаление у лиц с ожирением [33], вероятно, тоже подвергаясь модуляции АТФ-связывающей кассетой (ABC) экспрессии A1 или ABCG1 в мононуклеарных клетках периферической крови (PBMC) [89]. Другой мета-анализ показал, что чеснок обладает кардиопротекторным действием, снижая уровни холестерина и ТГ в сыворотке крови у пациентов с умеренной гиперхолестеринемией [90].
Наконец, несмотря на то что несколько экспериментальных исследований показали, что чеснок обладает антитромбоцитарными свойствами, рандомизированное клиническое исследование показало, что чесночное масло и таблетки практически не влияют на агрегацию тромбоцитов и оказывают умеренное побочное действие в виде увеличения кровоточивости у некоторых испытуемых добровольцев, даже если доза таблеток может быть эквивалентна дозе кардиопротективного средства аспирин [91,92]. Таким образом, значительное внимание уделяется обеспечению применения экстракта чеснока GE вместе пероральной антикоагулянтной терапией. Двойное слепое рандомизированное плацебо-контролируемое пилотное исследование показало, что 5 мл AGE два раза в день могут быть безопасны для пациентов с кровотечениями в сочетании с терапией варфарином [93]. Артериальное давлениеГипертония развивается, когда когда кровь оказывает давление на стенки кровеносных сосудов или артерий [98]. Недавно чеснок продемонстрировал удовлетворительный эффект в качестве средства от гипертонии, регулируя высокий уровень холестерина и стимулируя иммунную систему [99]. В исследовании "доза-эффект" сообщалось, что AGE оказывал антигипертензивное действие, снижая систолическое артериальное давление в случае неконтролируемой гипертонической болезни без каких-либо заметных побочных эффектов [100]. Более того, у пациентов с умеренной гиперхолестеринемией приём экстрактов AGE или сухого чесночного порошка в дозе 7,2 г в день в течение четырёх недель умеренно снижал систолическое артериальное давление (САД) и диастолическое артериальное давление (ДАД) (на 5,5%) за счёт снижения сывороточного ТС и ЛПНП, даже если не было обнаружено заметных изменений в уровне ЛПВП по сравнению с группой плацебо [101,102]. Аналогичный результат наблюдался у пациентов с метаболическим синдромом при приёме сырого измельчённого чеснока в дозе 100 мг/кг два раза в день на протяжении 4 недель, было зафиксировано снижение САД и ДАД за счёт снижения уровня ТГ и повышения уровня холестерина ЛПВП в сыворотке крови [96]. Кроме того, при рационе на основе чесночного гомогената в дозе 300 мг в день в течение 12 недель наблюдалось значительное снижение показателей САД и ДАД у пациентов с умеренной артериальной гипертензией, но не у пациентов с предгипертензией; побочных эффектов не было выявлено [103].
Кроме того, совместное употребление чеснока и кориандра оказывало значительное влияние на липидный профиль, при этом потребление чеснока, кориандра или их смеси в дозе 2 г в день сильно влияло на индекс массы тела, уровень холестерина, ЛПНП и ЛПВП и снижало артериального давления у пациентов с артериальной гипертензией [104]. Напротив, Саймонс и соавт. не обнаружили существенного влияния приёма чеснока на уровень липидов и липопротеинов у пациентов с умеренной гиперхолестеринемией [105].Сахарный диабетСахарный диабет является одним из основных неинфекционных хронических и широко распространённых заболеваний, представляющих угрозу для жизни. Диабет возникает вследствие абсолютного или относительного дефицита или резистентности к инсулину [79]. Данное хроническое заболевание очень распространено в популяции, при этом число диабетиков в мире за последние три десятилетия увеличилось в четыре раза [106,107]. По оценкам Международной диабетической федерации в 2015 году диабетом страдали 415 миллионов взрослых, и, по прогнозам, к 2040 году этот показатель достигнет 642 миллиона [108]. Окислительный стресс ответственен за развитие диабета. Доклинические исследования показали, что активные сераорганические соединения чеснока снижают гипергликемию за счет улучшения антиоксидантного статуса кровообращения у крыс с диабетом [106]. Кроме того, компонент чеснока выступает в качестве донора сероводорода, который также контролирует диабет 2 типа [109]. Недавно проведенные мета-анализы продемонстрировали, что чеснок может снижать липидный профиль и такие показатели глюкозы как уровень глюкозы в крови натощак [110,111] и уровень гемоглобина A1c (HbA1c) у пациентов с сахарным диабетом [112]. Кроме того, приём 300 мг чесночной добавки два раза в день в течение 12 недель значительно улучшил показатели сыворотки крови., уровень ТГ, ХС и ЛПНП и снижал уровень липидов в сыворотке крови по сравнению с пациентами с сахарным диабетом из группы плацебо, с неконтролируемой дислипидемией [113]. Более того, комбинация противодиабетического препарата метформина в дозировке 500 мг два раза в день с чесноком по 300 мг три раза в день в течение 24 недель имели больший потенциал в лечении пациентов с сахарным диабетом за счет снижения общего холестерина, ЛПНП и ТГ и улучшения гиперлипидемии [114]. С другой стороны, двойное слепое плацебо-контролируемое перекрёстное пилотное исследование показало, что AGE не оказывает существенного влияния на резистентность к инсулину при приёме 1200 мг в день в течение четырёх недель у взрослых с сахарным диабетом 2 типа [37]. Наконец, двойное слепое клиническое исследование на пациентах с сахарным диабетом показало, что фитотерапия чесноком в дозе 750 мг 3 раза в день в течение 12 недель потенциально эффективна при лечении диабета за счёт снижения уровня глюкозы в крови натощак посредством снижения уровня HbA1 [115].Заболевания костейОстеоартрит (ОА) — это обширное дегенеративное заболевание костных суставов, связанное с хронической и инвалидизирующей болью, в патогенезе которого особую роль играют адипоцитокины, резистин и провоспалительные маркеры [116]. Было показано, что прием пищевой добавки, содержащей чеснок, в дозе 1000 мг в день в течение 12 недель эффективен для облегчения симптомов у женщин с избыточным весом или ожирением, страдающих остеоартрозом коленного сустава [117]. Более того, приём таблеток с чесноком по 500 мг два раза в день в течение 12 недель продемонстрировал противовоспалительный и обезболивающий эффекты за счёт снижения концентрации резистина и TNF-α в сыворотке крови, а также снизил выраженность боли у женщин с ОА коленного сустава, страдающих ожирением или избыточным весом [116].
Другое рандомизированное клиническое исследование показало, что таблетки с чесноком действуют как антиоксидант у женщин с остеопорозом в постменопаузе. В этом исследовании было обнаружено значительное снижение уровня белковых продуктов повышенного окисления и карбонильных веществ в плазме крови и сопутствующее повышение TAC, а также снижение окислительного стресса и остеопороза после употребления чесночных таблеток в дозе 2 таблетки (что эквивалентно 2 г свежего чеснока) в день в течение 12 месяцев [118]. Кроме того, была выявлена взаимосвязь между активностью провоспалительных цитокинов и приёмом таблеток с чесноком два раза в день в течение восьми месяцев при потере костной массы в постменопаузе, когда чеснок модулировал выработку цитокинов и снижал проявление остеопороза у женщин с остеопорозом в постменопаузе [36].Кожные заболеванияЧеснок уже давно используется в традиционной и комплементарной медицине [119], и несколько клинических испытаний продемонстрировали эффективность его применения при устранении симптомов, связанных с бородавками [120], зубным стоматитом [121], венозными язвами [122] и кожными ранами [85,123]. Например, в доклинических исследованиях AGE показал способность к заживлению ран в зависимости от дозы после шестидневного применения [123,124].
Лечение вируса бородавок путём улучшения состояния иммунной системы может быть достигнуто с помощью внутриочаговой иммунотерапии [125,126], и это может привести к воздействию на все язвы на теле [127]. Рандомизированное контрольное исследование показало, что применение липидной части экстракта чеснока GE два раза в день в течение четырёх недель оказывало значительное воздействие на пациентов с рецидивирующими множественными бородавками по сравнению с другими формами лечения посредством модуляции уровня TNF-α в сыворотке крови и продвижением иммунотерапии [120]. Аналогичным образом, зубной стоматит является распространённой формой хронического кандидоза полости рта, и рандомизированное клиническое исследование показало, что GE в дозе 40 мг/мл три раза в день потенциально может заменить лечения зубного стоматита нистатином [121]. Наконец, было проведено проспективное нерандомизированное пилотное исследование на пациентах с венозной язвой, использующих травяную мазь, содержащую чеснок, обладающую противоэритематическим, эпителизирующим и противоотечным свойством; площадь венозной язвы уменьшилась после семи недель применения [122]. Другие заболеванияВ последние годы устойчивость микроорганизмов к антибиотикам стала серьёзной проблемой, поэтому значительное внимание уделяется антимикробной активности специй, таких как чеснок, из-за их ингибирующего действия на патогенные вирусы [128], бактерии [129], дрожжи [130] и грибы [131]. Антимикробный механизм чеснока может включать в себя ингибирование внеклеточных ферментов, лишение субстратов, необходимых для роста микроорганизмов, морфологические изменения и снижение адгезии бактерий к эпителиальным клеткам [132]. Например, рандомизированное двойное слепое контролируемое клиническое исследование выявило обратную связь между Streptococcus mutans, Lactobacilli и Candida albicans и ополаскивателями для полости рта, содержащими чеснок с лаймом, у детей с тяжёлой формой раннего кариеса [133]. Кроме того, было показано, что чесночные таблетки Гарцин в дозе 1500 мг в день в течение семи дней эффективны для лечения кандидозного вагинита вместо флуконазола у женщин с вагинитом [134]. Напротив, другое рандомизированное плацебо-контролируемое двойное слепое исследование показало неблагоприятное воздействие чеснока на бессимптомных женщин с положительным результатом посева на количество колоний candida во влагалище при приёме таблеток чеснока по 350 мг два раза в день [135]. Более того, в случае острой респираторной вирусной инфекции приём чесночных таблеток Алликор по 600 мг в день в течение пяти месяцев снижал частоту острых респираторных заболеваний в 2-4 раза на первом этапе и в 1,7 раза на втором этапе по сравнению с контролем, что приводит к подавлению инфекции [136].
Чесночные таблетки в дозе 400 мг в день также являются перспективным средством при внутрибольничных инфекциях у пациентов в отделениях интенсивной терапии и могут быть использованы для профилактики сепсиса и инфекций мочевыводящих путей после шести дней лечения [137]. Кроме того, лабораторные исследования и клинические испытания показали, что GE содержит сераорганические соединения, которые проявляют антилейшманиозную и иммуномодулирующую активность [138]. Например, гель для наружного применения с чесноком проявил антилейшманиозную активность у пациентов с кожным лейшманиозом и устранил повреждения кожи после применения в течение шести и восьми недель [139]. Напротив, другое пилотное рандомизированное контролируемое исследование капсул с чесноком не показало существенного эффекта при незначительных побочных эффектах в отношении чувства кворума синегнойной палочки у пациентов с муковисцидозом после ежедневного применения в течение восьми недель [140].
Употребление чеснока также оказывает защитное действие при заболеваниях желудка [141]. Панджешахин и др. провели метаанализ ферментов печени человека и показали, что добавление чеснока значительно снижает уровень фермента печени аспартаттрансферазы, не оказывая никакого влияния на уровень аланинаминотрансферазы (АЛТ) [142]. Кроме того, приём 1,5 г ферментированного GE в день эффективно и безопасно улучшал функцию печени за счёт повышения уровня сывороточной гамма-глутамилтранспептидазы (ГГТ) и АЛТ у взрослых пациентов в течение 12 недель [141]. Аналогично, препарат с чесноком диметил-4, 4’-диметокси-5, 6, 5’, 6’-диметилендиоксибифенил-2, 2’-дикарбоксилат (DDB) плюс чесночное масло (GO) после перорального применения оказывал значительный гепатопротекторный эффект у пациентов с хроническим гепатитом. Кроме того, шестинедельный курс лечения препаратом DDB plus GO по три-шесть капсул в день снижал уровень АЛТ в сыворотке крови и улучшал течение хронического гепатита [143]. Наконец, популяционное исследование показало, что частое употребление сырого чеснока обратно пропорционально связано с безалкогольным ожирением печени (БОП). У пациентов с БОП потребление чесночного порошка влияло на компоненты организма за счёт снижения массы тела и жировой массы [144,145].
Несколько эпидемиологических исследований, проведённых среди населения Китая, выявили значительную обратную зависимость между потреблением сырого чеснока или его компонентов - 8,4 г или 33,4 г в неделю в течение семи лет и раком лёгких [74]. Наконец, экстракт чеснока GE продемонстрировал профилактический эффект в отношении фебрильной нейропатии после получения химиотерапии у пациентов с гематологическими злокачественными новообразованиями, потенциально снижая риск связанной с химиотерапией фебрильной нейтропении после приёма GE в дозе 900 мг в день в течение трех недель по сравнению с плацебо [75].
В качестве объяснений химиопрофилактических эффектов чеснока используются многочисленные механизмы, включая ингибирование образования аддуктов ДНК, ингибирование мутагенеза путём блокирования метаболизма, посредством удаления свободных радикалов или путём уменьшения пролиферации клеток и роста опухолей [74]. В этом контексте Чаррон и соавт. [76] провели клиническое исследование экспрессии генов, связанных с иммунитетом, апоптозом и метаболизмом ксенобиотиков у людей, после ежедневного употребления 5 г сырого измельчённого чеснока в течение 10 дней. Однократный приём пищи, содержащий сырой измельчённый чеснок, активизировал экспрессию семи генов, таких как активирующий белок с мотивом активации иммунорецептора на основе тирозина 1, ядерный транслокатор арилуглеводородного рецептора, арилуглеводородный рецептор, индуцируемый гипоксией фактор 1α, c-Jun, ядерный фактор активированные Т-клетки, онкостатин M и гомолог вируса ретикулоэндотелиоза птиц V-rel в крови здоровых добровольцев, таким образом, подавляя онкогенез. Сердечно-сосудистые заболеванияВ настоящее время сердечно-сосудистые заболевания (ССЗ) являются основной причиной заболеваемости и смертности -во всем мире ежегодно умирает 17,3 миллиона человек, и ожидается, что к 2030 году это число превысит 23,6 миллиона [77]. Многие факторы риска влияют на развитие сердечно-сосудистых заболеваний, включая сахарный диабет 2 типа, ожирение, резистентность к инсулину, высокое артериальное давление, метаболический синдром, высокий уровень триглицеридов в сыворотке крови и липидный профиль плазмы [78]. Согласно современным исследованиям, чеснок, благодаря синергическому действию его питательных и фитохимических компонентов, может значительно снизить риск развития атеросклероза, гипертонии, диабета, гиперлипидемии, инфаркта миокарда и ишемического инсульта [79]. Например, атеросклероз и воспаление сосудов обычно сопровождаются окислительным стрессом, дисфункцией эндотелия и выработкой воспалительных цитокинов [80,81]. С точки зрения диетического подхода чеснок играет потенциальную роль в профилактике и лечении атеросклероза и инфаркта миокарда [82,83], что было продемонстрировано в рандомизированном исследовании, проведённом с использованием выдержанного экстракта чеснока AGE и суррогата жировой ткани при прогрессирующем коронарном атеросклерозе. В исследовании сообщалось об уменьшении роста коронарного атеросклероза при приеме 250 мг AGE ежедневно в течение 12 месяцев за счёт уменьшения эпикардиальной жировой ткани, перикардиальной жировой ткани, периаортальной жировой ткани и подкожной жировой ткани [84]. Кроме того, AGE предотвращал процесс развития атеросклероза, улучшая микроциркуляцию у пациентов в дозе 2400 мг AGE в сутки [85]. Более того, растительный препарат чеснока, богатый изофлавоноидами, в 1,5 раза замедлял прогрессирование атеросклероза у женщин в постменопаузе в дозе 500 мг в течение 12 месяцев после приема [86]. Другое рандомизированное двойное слепое исследование продемонстрировало, что приём 2400 мг AGE в день в течение 52 недель уменьшал количество бляшек в коронарных артериях у пациентов с метаболическим синдромом [87], но существенного влияния на уровень липопротеидов выявлено не было [88]. С другой стороны, приём AGE в дозе 6 г ежедневно в течение 12 недель снижал уровень липопротеина В и повышал уровень ЛПВП, демонстрируя кардиопротекторный эффект у пациентов с умеренной гиперхолестеринемией [55]. Кроме того, GE, принимаемый в дозе 400 мг в день в течение трех месяцев, изменял маркеры функции эндотелия, такие как hs-CRP, PAI-1, холестерин (общий, ЛПНП, ЛПВП) и триглицериды, а также подавлял хроническое воспаление у лиц с ожирением [33], вероятно, тоже подвергаясь модуляции АТФ-связывающей кассетой (ABC) экспрессии A1 или ABCG1 в мононуклеарных клетках периферической крови (PBMC) [89]. Другой мета-анализ показал, что чеснок обладает кардиопротекторным действием, снижая уровни холестерина и ТГ в сыворотке крови у пациентов с умеренной гиперхолестеринемией [90].
Наконец, несмотря на то что несколько экспериментальных исследований показали, что чеснок обладает антитромбоцитарными свойствами, рандомизированное клиническое исследование показало, что чесночное масло и таблетки практически не влияют на агрегацию тромбоцитов и оказывают умеренное побочное действие в виде увеличения кровоточивости у некоторых испытуемых добровольцев, даже если доза таблеток может быть эквивалентна дозе кардиопротективного средства аспирин [91,92]. Таким образом, значительное внимание уделяется обеспечению применения экстракта чеснока GE вместе пероральной антикоагулянтной терапией. Двойное слепое рандомизированное плацебо-контролируемое пилотное исследование показало, что 5 мл AGE два раза в день могут быть безопасны для пациентов с кровотечениями в сочетании с терапией варфарином [93]. Артериальное давлениеГипертония развивается, когда когда кровь оказывает давление на стенки кровеносных сосудов или артерий [98]. Недавно чеснок продемонстрировал удовлетворительный эффект в качестве средства от гипертонии, регулируя высокий уровень холестерина и стимулируя иммунную систему [99]. В исследовании "доза-эффект" сообщалось, что AGE оказывал антигипертензивное действие, снижая систолическое артериальное давление в случае неконтролируемой гипертонической болезни без каких-либо заметных побочных эффектов [100]. Более того, у пациентов с умеренной гиперхолестеринемией приём экстрактов AGE или сухого чесночного порошка в дозе 7,2 г в день в течение четырёх недель умеренно снижал систолическое артериальное давление (САД) и диастолическое артериальное давление (ДАД) (на 5,5%) за счёт снижения сывороточного ТС и ЛПНП, даже если не было обнаружено заметных изменений в уровне ЛПВП по сравнению с группой плацебо [101,102]. Аналогичный результат наблюдался у пациентов с метаболическим синдромом при приёме сырого измельчённого чеснока в дозе 100 мг/кг два раза в день на протяжении 4 недель, было зафиксировано снижение САД и ДАД за счёт снижения уровня ТГ и повышения уровня холестерина ЛПВП в сыворотке крови [96]. Кроме того, при рационе на основе чесночного гомогената в дозе 300 мг в день в течение 12 недель наблюдалось значительное снижение показателей САД и ДАД у пациентов с умеренной артериальной гипертензией, но не у пациентов с предгипертензией; побочных эффектов не было выявлено [103].
Кроме того, совместное употребление чеснока и кориандра оказывало значительное влияние на липидный профиль, при этом потребление чеснока, кориандра или их смеси в дозе 2 г в день сильно влияло на индекс массы тела, уровень холестерина, ЛПНП и ЛПВП и снижало артериального давления у пациентов с артериальной гипертензией [104]. Напротив, Саймонс и соавт. не обнаружили существенного влияния приёма чеснока на уровень липидов и липопротеинов у пациентов с умеренной гиперхолестеринемией [105].Сахарный диабетСахарный диабет является одним из основных неинфекционных хронических и широко распространённых заболеваний, представляющих угрозу для жизни. Диабет возникает вследствие абсолютного или относительного дефицита или резистентности к инсулину [79]. Данное хроническое заболевание очень распространено в популяции, при этом число диабетиков в мире за последние три десятилетия увеличилось в четыре раза [106,107]. По оценкам Международной диабетической федерации в 2015 году диабетом страдали 415 миллионов взрослых, и, по прогнозам, к 2040 году этот показатель достигнет 642 миллиона [108]. Окислительный стресс ответственен за развитие диабета. Доклинические исследования показали, что активные сераорганические соединения чеснока снижают гипергликемию за счет улучшения антиоксидантного статуса кровообращения у крыс с диабетом [106]. Кроме того, компонент чеснока выступает в качестве донора сероводорода, который также контролирует диабет 2 типа [109]. Недавно проведенные мета-анализы продемонстрировали, что чеснок может снижать липидный профиль и такие показатели глюкозы как уровень глюкозы в крови натощак [110,111] и уровень гемоглобина A1c (HbA1c) у пациентов с сахарным диабетом [112]. Кроме того, приём 300 мг чесночной добавки два раза в день в течение 12 недель значительно улучшил показатели сыворотки крови., уровень ТГ, ХС и ЛПНП и снижал уровень липидов в сыворотке крови по сравнению с пациентами с сахарным диабетом из группы плацебо, с неконтролируемой дислипидемией [113]. Более того, комбинация противодиабетического препарата метформина в дозировке 500 мг два раза в день с чесноком по 300 мг три раза в день в течение 24 недель имели больший потенциал в лечении пациентов с сахарным диабетом за счет снижения общего холестерина, ЛПНП и ТГ и улучшения гиперлипидемии [114]. С другой стороны, двойное слепое плацебо-контролируемое перекрёстное пилотное исследование показало, что AGE не оказывает существенного влияния на резистентность к инсулину при приёме 1200 мг в день в течение четырёх недель у взрослых с сахарным диабетом 2 типа [37]. Наконец, двойное слепое клиническое исследование на пациентах с сахарным диабетом показало, что фитотерапия чесноком в дозе 750 мг 3 раза в день в течение 12 недель потенциально эффективна при лечении диабета за счёт снижения уровня глюкозы в крови натощак посредством снижения уровня HbA1 [115].Заболевания костейОстеоартрит (ОА) — это обширное дегенеративное заболевание костных суставов, связанное с хронической и инвалидизирующей болью, в патогенезе которого особую роль играют адипоцитокины, резистин и провоспалительные маркеры [116]. Было показано, что прием пищевой добавки, содержащей чеснок, в дозе 1000 мг в день в течение 12 недель эффективен для облегчения симптомов у женщин с избыточным весом или ожирением, страдающих остеоартрозом коленного сустава [117]. Более того, приём таблеток с чесноком по 500 мг два раза в день в течение 12 недель продемонстрировал противовоспалительный и обезболивающий эффекты за счёт снижения концентрации резистина и TNF-α в сыворотке крови, а также снизил выраженность боли у женщин с ОА коленного сустава, страдающих ожирением или избыточным весом [116].
Другое рандомизированное клиническое исследование показало, что таблетки с чесноком действуют как антиоксидант у женщин с остеопорозом в постменопаузе. В этом исследовании было обнаружено значительное снижение уровня белковых продуктов повышенного окисления и карбонильных веществ в плазме крови и сопутствующее повышение TAC, а также снижение окислительного стресса и остеопороза после употребления чесночных таблеток в дозе 2 таблетки (что эквивалентно 2 г свежего чеснока) в день в течение 12 месяцев [118]. Кроме того, была выявлена взаимосвязь между активностью провоспалительных цитокинов и приёмом таблеток с чесноком два раза в день в течение восьми месяцев при потере костной массы в постменопаузе, когда чеснок модулировал выработку цитокинов и снижал проявление остеопороза у женщин с остеопорозом в постменопаузе [36].Кожные заболеванияЧеснок уже давно используется в традиционной и комплементарной медицине [119], и несколько клинических испытаний продемонстрировали эффективность его применения при устранении симптомов, связанных с бородавками [120], зубным стоматитом [121], венозными язвами [122] и кожными ранами [85,123]. Например, в доклинических исследованиях AGE показал способность к заживлению ран в зависимости от дозы после шестидневного применения [123,124].
Лечение вируса бородавок путём улучшения состояния иммунной системы может быть достигнуто с помощью внутриочаговой иммунотерапии [125,126], и это может привести к воздействию на все язвы на теле [127]. Рандомизированное контрольное исследование показало, что применение липидной части экстракта чеснока GE два раза в день в течение четырёх недель оказывало значительное воздействие на пациентов с рецидивирующими множественными бородавками по сравнению с другими формами лечения посредством модуляции уровня TNF-α в сыворотке крови и продвижением иммунотерапии [120]. Аналогичным образом, зубной стоматит является распространённой формой хронического кандидоза полости рта, и рандомизированное клиническое исследование показало, что GE в дозе 40 мг/мл три раза в день потенциально может заменить лечения зубного стоматита нистатином [121]. Наконец, было проведено проспективное нерандомизированное пилотное исследование на пациентах с венозной язвой, использующих травяную мазь, содержащую чеснок, обладающую противоэритематическим, эпителизирующим и противоотечным свойством; площадь венозной язвы уменьшилась после семи недель применения [122]. Другие заболеванияВ последние годы устойчивость микроорганизмов к антибиотикам стала серьёзной проблемой, поэтому значительное внимание уделяется антимикробной активности специй, таких как чеснок, из-за их ингибирующего действия на патогенные вирусы [128], бактерии [129], дрожжи [130] и грибы [131]. Антимикробный механизм чеснока может включать в себя ингибирование внеклеточных ферментов, лишение субстратов, необходимых для роста микроорганизмов, морфологические изменения и снижение адгезии бактерий к эпителиальным клеткам [132]. Например, рандомизированное двойное слепое контролируемое клиническое исследование выявило обратную связь между Streptococcus mutans, Lactobacilli и Candida albicans и ополаскивателями для полости рта, содержащими чеснок с лаймом, у детей с тяжёлой формой раннего кариеса [133]. Кроме того, было показано, что чесночные таблетки Гарцин в дозе 1500 мг в день в течение семи дней эффективны для лечения кандидозного вагинита вместо флуконазола у женщин с вагинитом [134]. Напротив, другое рандомизированное плацебо-контролируемое двойное слепое исследование показало неблагоприятное воздействие чеснока на бессимптомных женщин с положительным результатом посева на количество колоний candida во влагалище при приёме таблеток чеснока по 350 мг два раза в день [135]. Более того, в случае острой респираторной вирусной инфекции приём чесночных таблеток Алликор по 600 мг в день в течение пяти месяцев снижал частоту острых респираторных заболеваний в 2-4 раза на первом этапе и в 1,7 раза на втором этапе по сравнению с контролем, что приводит к подавлению инфекции [136].
Чесночные таблетки в дозе 400 мг в день также являются перспективным средством при внутрибольничных инфекциях у пациентов в отделениях интенсивной терапии и могут быть использованы для профилактики сепсиса и инфекций мочевыводящих путей после шести дней лечения [137]. Кроме того, лабораторные исследования и клинические испытания показали, что GE содержит сераорганические соединения, которые проявляют антилейшманиозную и иммуномодулирующую активность [138]. Например, гель для наружного применения с чесноком проявил антилейшманиозную активность у пациентов с кожным лейшманиозом и устранил повреждения кожи после применения в течение шести и восьми недель [139]. Напротив, другое пилотное рандомизированное контролируемое исследование капсул с чесноком не показало существенного эффекта при незначительных побочных эффектах в отношении чувства кворума синегнойной палочки у пациентов с муковисцидозом после ежедневного применения в течение восьми недель [140].
Употребление чеснока также оказывает защитное действие при заболеваниях желудка [141]. Панджешахин и др. провели метаанализ ферментов печени человека и показали, что добавление чеснока значительно снижает уровень фермента печени аспартаттрансферазы, не оказывая никакого влияния на уровень аланинаминотрансферазы (АЛТ) [142]. Кроме того, приём 1,5 г ферментированного GE в день эффективно и безопасно улучшал функцию печени за счёт повышения уровня сывороточной гамма-глутамилтранспептидазы (ГГТ) и АЛТ у взрослых пациентов в течение 12 недель [141]. Аналогично, препарат с чесноком диметил-4, 4’-диметокси-5, 6, 5’, 6’-диметилендиоксибифенил-2, 2’-дикарбоксилат (DDB) плюс чесночное масло (GO) после перорального применения оказывал значительный гепатопротекторный эффект у пациентов с хроническим гепатитом. Кроме того, шестинедельный курс лечения препаратом DDB plus GO по три-шесть капсул в день снижал уровень АЛТ в сыворотке крови и улучшал течение хронического гепатита [143]. Наконец, популяционное исследование показало, что частое употребление сырого чеснока обратно пропорционально связано с безалкогольным ожирением печени (БОП). У пациентов с БОП потребление чесночного порошка влияло на компоненты организма за счёт снижения массы тела и жировой массы [144,145].
Заключение и перспективы В настоящей работе подчеркивается, что чеснок показал многообещающие свойства для профилактики и лечения различных заболеваний. Данный обзор суммирует противораковые, кардиопротективные, антигипергликемические, противомикробные, противогипертензивные и прочие эффекты чеснока или соединений с ним, которые обусловлены антиоксидантной, противовоспалительной и гиполипидемической активностью (Рис. 2)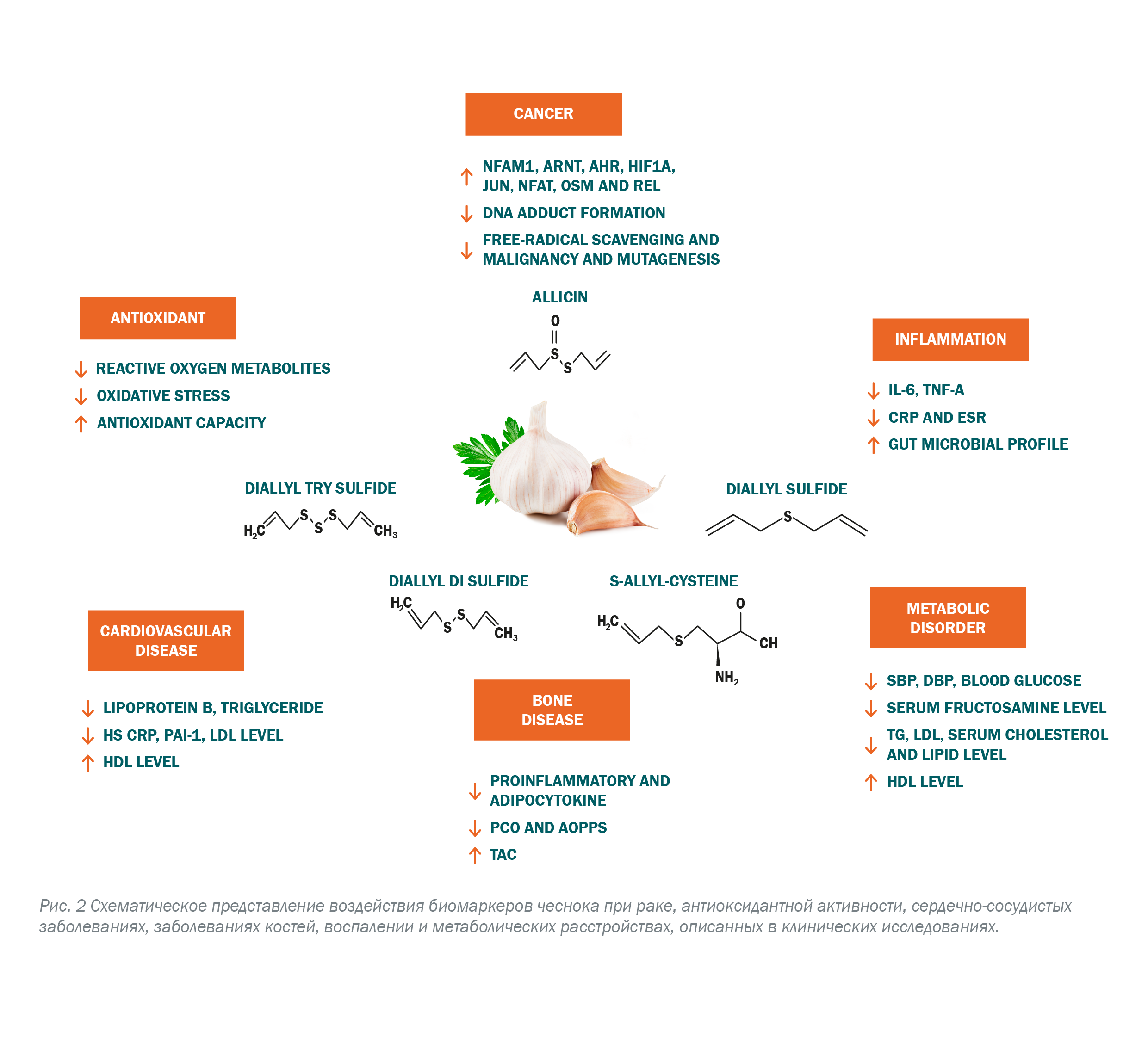 Как описано, чеснок разными способами может изменять некоторые биомаркеры при различных заболеваниях. Тем не менее, для лучшего понимания механизма его воздействия и получения более точных данных необходимо провести крупные, продолжительные, полностью ослепленные и хорошо контролируемые исследования. Кроме этого, необходимо провести дальнейшие исследования фармакокинетики и фармакодинамики на людях; например: фармакологически активные концентрации чесночных соединений серы в препаратах с чесноком, которые можно получить путем перорального приема или через фармакологические вмешательства. Более того, терапевтический прием чеснока ограничен из-за его быстрого метаболизма и плохой биодоступности. Для получения новой дозировки чеснока необходимо сконцентрироваться на улучшении его биодоступности. Наконец, существует ограниченные клинические данные о применении чеснока при таких нейродегенеративных расстройствах, как: Альцгеймер, болезнь Паркинсона, болезнь Хантингтона и амиотрофический латеральный склероз. Настоящий обзор может помочь в будущих исследованиях применения чеснока в медицине, благодаря его положительному влиянию на здоровье.
Как описано, чеснок разными способами может изменять некоторые биомаркеры при различных заболеваниях. Тем не менее, для лучшего понимания механизма его воздействия и получения более точных данных необходимо провести крупные, продолжительные, полностью ослепленные и хорошо контролируемые исследования. Кроме этого, необходимо провести дальнейшие исследования фармакокинетики и фармакодинамики на людях; например: фармакологически активные концентрации чесночных соединений серы в препаратах с чесноком, которые можно получить путем перорального приема или через фармакологические вмешательства. Более того, терапевтический прием чеснока ограничен из-за его быстрого метаболизма и плохой биодоступности. Для получения новой дозировки чеснока необходимо сконцентрироваться на улучшении его биодоступности. Наконец, существует ограниченные клинические данные о применении чеснока при таких нейродегенеративных расстройствах, как: Альцгеймер, болезнь Паркинсона, болезнь Хантингтона и амиотрофический латеральный склероз. Настоящий обзор может помочь в будущих исследованиях применения чеснока в медицине, благодаря его положительному влиянию на здоровье.
 Как описано, чеснок разными способами может изменять некоторые биомаркеры при различных заболеваниях. Тем не менее, для лучшего понимания механизма его воздействия и получения более точных данных необходимо провести крупные, продолжительные, полностью ослепленные и хорошо контролируемые исследования. Кроме этого, необходимо провести дальнейшие исследования фармакокинетики и фармакодинамики на людях; например: фармакологически активные концентрации чесночных соединений серы в препаратах с чесноком, которые можно получить путем перорального приема или через фармакологические вмешательства. Более того, терапевтический прием чеснока ограничен из-за его быстрого метаболизма и плохой биодоступности. Для получения новой дозировки чеснока необходимо сконцентрироваться на улучшении его биодоступности. Наконец, существует ограниченные клинические данные о применении чеснока при таких нейродегенеративных расстройствах, как: Альцгеймер, болезнь Паркинсона, болезнь Хантингтона и амиотрофический латеральный склероз. Настоящий обзор может помочь в будущих исследованиях применения чеснока в медицине, благодаря его положительному влиянию на здоровье.
Как описано, чеснок разными способами может изменять некоторые биомаркеры при различных заболеваниях. Тем не менее, для лучшего понимания механизма его воздействия и получения более точных данных необходимо провести крупные, продолжительные, полностью ослепленные и хорошо контролируемые исследования. Кроме этого, необходимо провести дальнейшие исследования фармакокинетики и фармакодинамики на людях; например: фармакологически активные концентрации чесночных соединений серы в препаратах с чесноком, которые можно получить путем перорального приема или через фармакологические вмешательства. Более того, терапевтический прием чеснока ограничен из-за его быстрого метаболизма и плохой биодоступности. Для получения новой дозировки чеснока необходимо сконцентрироваться на улучшении его биодоступности. Наконец, существует ограниченные клинические данные о применении чеснока при таких нейродегенеративных расстройствах, как: Альцгеймер, болезнь Паркинсона, болезнь Хантингтона и амиотрофический латеральный склероз. Настоящий обзор может помочь в будущих исследованиях применения чеснока в медицине, благодаря его положительному влиянию на здоровье. Johura Ansary 1,y, Tamara Yuliett Forbes-Hernández 2,y, Emilio Gil 3 , Danila Cianciosi 1 ,
Jiaojiao Zhang 1, Maria Elexpuru-Zabaleta 4 , Jesus Simal-Gandara 5 ,
Francesca Giampieri 1,2,6,* and Maurizio Battino 1,2,7,*1 Dipartimento di Scienze Cliniche Specialistiche e Odontostomtologiche—Università Politecnica delle
Marche, Via Ranieri 65, 60130 Ancona, Italy; j.ansary@pm.univpm.it (J.A.); d.cianciosi@pm.univpm.it (D.C.);
j.zhang@pm.univpm.it (J.Z.)
2 Nutrition and Food Science Group, department of Analytical and Food Chemistry, CITACA, CACTI,
University of Vigo-Vigo Campus, 36310 Vigo, Spain; tforbes@uvigo.es
3 Nutrition and Food Science Group, Department of Biochemistry, Genetics and Immunology,
Faculty of Biology, University of Vigo, 36310 Vigo, Spain; egil@uvigo.es
4 Dipartimento di Scienze Cliniche e Molecolari, Facoltà di Medicina, Università Politecnica delle Marche,
60131 Ancona, Italy; p015008@sta_.univpm.it
5 Nutrition and Bromatology Group, Department of Analytical and Food Chemistry, Faculty of Science,
University of Vigo, Ourense Campus, E-32004 Ourense, Spain; jsimal@uvigo.es
6 College of Food Science and Technology, Northwest University, Xi’an, Shaanxi 710069, China
7 International Research Center for Food Nutrition and Safety, Jiangsu University, Zhenjiang 212013, China
Эти авторы внесли равный вкладВклад авторов: концептуализация – J.A и T.Y.F.-H; написание – подготовка финального варианта J.A и T.Y.F.-H и D.C.; цифры и таблицы – J.Z. и M.E.-Z; написание – правки и рецензирование – E.G. и J.S. -G; контроль – M.B. Все авторы прочитали и согласны с опубликованным материалом. Бюджет: без внешнего финансирования. Благодарности: T.Y.F.-H работает с «Juan de la Cierva-Formacio`n» (постдокторантурный контракт). Конфликт интересов: авторы не сообщают о конфликте интересов. Список литературы1. Jiang, T.A. Health Benefits of Culinary Herbs and Spices. J. AOAC Int. 2019, 102, 395–411. [CrossRef] [PubMed]
2. Petrovska, B.B.; Cekovska, S. Extracts from the history and medical properties of garlic. Pharmacogn. Rev. 2010, 4, 106–110. [CrossRef] [PubMed]
3. Setiawan, V.W.; Yu, G.P.; Lu, Q.Y.; Lu, M.L.; Yu, S.Z.; Mu, L.; Zhang, J.G.; Kurtz, R.C.; Cai, L.; Hsieh, C.C.; et al. Allium vegetables and stomach cancer risk in China. Asian Pac. J. Cancer Prev. APJCP 2005, 6, 387–395.
4. Diretto, G.; Rubio-Moraga, A.; Argandoña, J.; Castillo, P.; Gómez-Gómez, L.; Ahrazem, O. Tissue-specific accumulation of sulfur compounds and saponins in different parts of garlic cloves from purple and white ecotypes. Molecules 2017, 22, 1359. [CrossRef] [PubMed]
5. Gorinstein, S.; Leontowicz, H.; Leontowicz, M.; Namiesnik, J.; Najman, K.; Drzewiecki, J.; Cvikrová, M.; Martincová, O.; Katrich, E.; Trakhtenberg, S. Comparison of the main bioactive compounds and antioxidant activities in garlic and white and red onions after treatment protocols. J. Agric. Food Chem. 2008, 56, 4418–4426.
[CrossRef] [PubMed]
6. Wang, Y.; Guan, M.; Zhao, X.; Li, X. Effects of garlic polysaccharide on alcoholic liver fibrosis and intestinal microflora in mice. Pharm. Biol. 2018, 56, 325–332. [CrossRef]
7. Liang, J.J.; Li, H.R.; Chen, Y.; Zhang, C.; Chen, D.G.; Liang, Z.C.; Shi, Y.Q.; Zhang, L.L.; Xin, L.; Zhao, D.B. Diallyl Trisulfide can induce fibroblast-like synovial apoptosis and has a therapeutic effect on collagen-induced arthritis in mice via blocking NF-B and Wnt pathways. Int. Immunopharmacol. 2019, 71, 132–138. [CrossRef]
8. Jiang, X.Y.; Zhu, X.S.; Xu, H.Y.; Zhao, Z.X.; Li, S.Y.; Li, S.Z.; Cai, J.H.; Cao, J.M. Diallyl trisulfide suppresses tumor growth through the attenuation of Nrf2/Akt and activation of p38/JNK and potentiates cisplatin efficacy in gastric cancer treatment. Acta Pharmacol. Sin. 2017, 38, 1048–1058. [CrossRef]
9. Lv, Y.; So, K.-F.; Wong, N.-K.; Xiao, J. Anti-cancer activities of S-allylmercaptocysteine from aged garlic. Chin. J. Nat. Med. 2019, 17, 43–49. [CrossRef]
10. Ohtani, M.; Nishimura, T. Sulfur-containing amino acids in aged garlic extract inhibit inflammation in human gingival epithelial cells by suppressing intercellular adhesion molecule-1 expression and IL-6 secretion. Biomed. Rep. 2020, 12, 99–108. [CrossRef]
11. Kiesel, V.A.; Stan, S.D. Diallyl trisulfide, a chemopreventive agent from Allium vegetables, inhibits alpha-secretases in breast cancer cells. Biochem. Biophys. Res. Commun. 2017, 484, 833–838. [CrossRef]
12. Lu, J.; Cheng, B.; Meng, Z.; Fang, B.; Li, T.; Sun, M.; Liu, M.; Guan, S. Alliin attenuates 1, 3-dichloro-2-propanol-induced lipogenesis in HepG2 cells through activation of the AMP-activated protein
kinase-dependent pathway. Life Sci. 2018, 195, 19–24. [CrossRef]
13. Wang, M.J.; Cai, W.J.; Zhu, Y.C. Mechanisms of angiogenesis: Role of hydrogen sulphide. Clin. Exp. Pharmacol. Physiol. 2010, 37, 764–771. [CrossRef]
14. Kong, F.; Lee, B.H.;Wei, K. 5-Hydroxymethylfurfural Mitigates Lipopolysaccharide-Stimulated Inflammation via Suppression of MAPK, NF-B and mTOR Activation in RAW 264.7 Cells. Molecules 2019, 24, 275. [CrossRef] [PubMed]
15. Padiya, R.; Chowdhury, D.; Borkar, R.; Srinivas, R.; Bhadra, M.P.; Banerjee, S.K. Garlic attenuates cardiac oxidative stress via activation of PI3K/AKT/Nrf2-Keap1 pathway in fructose-fed diabetic rat. PLoS ONE 2014, 9, e94228. [CrossRef] [PubMed]
16. Alma, E.; Eken, A.; Ercil, H.; Yelsel, K.; Daglioglu, N. The effect of garlic powder on human urinary cytokine excretion. Urol. J. 2014, 11, 1308–1315.
17. Lawson, L.D.; Gardner, C.D. Composition, stability, and bioavailability of garlic products used in a clinical trial. J. Agric. Food Chem. 2005, 53, 6254–6261. [CrossRef]
18. Agarwal, K.C. Therapeutic actions of garlic constituents. Med. Res. Rev. 1996, 16, 111–124. [CrossRef]
19. Gu, C.; Howell, K.; Dunshea, F.R.; Suleria, H.A. Lc-esi-qtof/ms characterisation of phenolic acids and flavonoids in polyphenol-rich fruits and vegetables and their potential antioxidant activities. Antioxidants 2019, 8, 405. [CrossRef] [PubMed]
20. Dziri, S.; Hassen, I.; Fatnassi, S.; Mrabet, Y.; Casabianca, H.; Hanchi, B.; Hosni, K. Phenolic constituents, antioxidant and antimicrobial activities of rosy garlic (Allium roseum var. odoratissimum). J. Funct. Foods 2012, 4, 423–432. [CrossRef]
21. Fenwick, G.R.; Hanley, A.B.; Whitaker, J.R. The genus allium. Part 2. Crit. Rev. Food Sci. Nutr. 1985, 22, 273–377. [CrossRef] [PubMed]
22. Londhe, V.P. Role of garlic (Allium sativum) in various diseases: An overview. Angiogenesis 2011, 12, 13.
23. Rana, S.V.; Pal, R.; Vaiphei, K.; Sharma, S.K.; Ola, R.P. Garlic in health and disease. Nutr. Res. Rev. 2011, 24, 60–71. [CrossRef] [PubMed]
24. Lawson, L.D.; Hunsaker, S.M. Allicin bioavailability and bioequivalence from garlic supplements and garlic foods. Nutrients 2018, 10, 812. [CrossRef]
25. Lawson, L.D.; Ransom, D.K.; Hughes, B.G. Inhibition of whole blood platelet-aggregation by compounds in garlic clove extracts and commercial garlic products. Thromb. Res. 1992, 65, 141–156. [CrossRef]
26. Freeman, F.; Kodera, Y. Garlic chemistry: Stability of S-(2-propenyl)-2-propene-1-sulfinothioate (allicin) in blood, solvents, and simulated physiological fluids. J. Agric. Food Chem. 1995, 43, 2332–2338. [CrossRef]
27. Germain, E.; Auger, J.; Ginies, C.; Siess, M.H.; Teyssier, C. In vivo metabolism of diallyl disulphide in the rat: Identification of two new metabolites. Xenobiotica 2002, 32, 1127–1138. [CrossRef]
28. Nagae, S.; Ushijima, M.; Hatono, S.; Imai, J.; Kasuga, S.; Matsuura, H.; Itakura, Y.; Higashi, Y. Pharmacokinetics of the garlic compound S-allylcysteine. Planta Med. 1994, 60, 214–217. [CrossRef]
29. Berginc, K.; Milisav, I.; Kristl, A. Garlic flavonoids and organosulfur compounds: Impact on the hepatic pharmacokinetics of saquinavir and darunavir. Drug Metab. Pharmacokinet. 2010, 25, 521–530. [CrossRef]
30. Miraghajani, M.; Rafie, N.; Hajianfar, H.; Larijani, B.; Azadbakht, L. Aged garlic and cancer: A systematic review. Int. J. Prev. Med. 2018, 9, 84.
31. Petropoulos, S.; Fernandes, Â.; Barros, L.; Ciric, A.; Sokovic, M.; Ferreira, I.C. Antimicrobial and antioxidant properties of various Greek garlic genotypes. Food Chem. 2018, 245, 7–12. [CrossRef] [PubMed]
32. Tsuneyoshi, T. BACH1 mediates the antioxidant properties of aged garlic extract. Exp. Ther. Med. 2020, 1500–1503. [CrossRef]
33. Szulin´ ska, M.; Kre˛gielska-Naroz˙na, M.; S´wia˛tek, J.; Stys´, P.; Kuz´nar-Kamin´ ska, B.; Jakubowski, H.; Walkowiak, J.; Bogda´ nski, P. Garlic extract favorably modifies markers of endothelial function in obese patients–randomized double blind placebo-controlled nutritional intervention. Biomed. Pharmacother. 2018, 102, 792–797. [CrossRef]
34. Mirunalini, S.; Krishnaveni, M.; Ambily, V. E effects of raw garlic (Allium sativum) on hyperglycemia in patients with type 2 diabetes mellitus. Pharmacologyonline 2011, 2, 968–974.
35. Moosavian, S.P.; Arab, A.; Paknahad, Z.; Moradi, S. The effects of garlic supplementation on oxidative stress markers: A systematic review and meta-analysis of randomized controlled trials. Complement. Ther. Med. 2020, 50, 102385. [CrossRef] [PubMed]
36. Ahmadian, F.; Moza ari-Khosravi, H.; Azaraein, M.H.; Faraji, R.; Zavar-Reza, J. The effect of consumption of garlic tablet on proteins oxidation biomarkers in postmenopausal osteoporotic women: A randomized clinical trial. Electron. Physician 2017, 9, 5670–5675. [CrossRef] [PubMed]
37. Khoobkhahi, N.; Delavar, R.; Nayebifar, S.H. The combinatory effects of combined training (endurance–resistance) and garlic supplementation on oxidative stress and antioxidant adaptations in untrained boys. Sci. Sports 2019, 34, 410.e1–410.e7. [CrossRef]
38. Atkin, M.; Laight, D.; Cummings, M.H. The effects of garlic extract upon endothelial function, vascular inflammation, oxidative stress and insulin resistance in adults with type 2 diabetes at high cardiovascular risk. A pilot double blind randomized placebo controlled trial. J. Diabetes Complicat 2016, 30, 723–727. [CrossRef]
39. Williams, M.J.; Sutherland,W.H.; McCormick, M.P.; Yeoman, D.J.; De Jong, S.A. Aged garlic extract improves endothelial function in men with coronary artery disease. Phytother. Res. 2005, 19, 314–319. [CrossRef]
40. Lee, G.Y.; Lee, J.J.; Lee, S.M. Antioxidant and anticoagulant status were improved by personalized dietary intervention based on biochemical and clinical parameters in cancer patients. Nutr. Cancer 2015, 67, 1083–1092. [CrossRef] McCrea, C.E.; West, S.G.; Kris-Etherton, P.M.; Lambert, J.D.; Gaugler, T.L.; Teeter, D.L.; Sauder, K.A.; Gu, Y.; Glisan, S.L.; Skulas-Ray, A.C. E_ects of culinary spices and psychological stress on postprandial lipemia and lipase activity: Results of a randomized crossover study and in vitro experiments. J. Transl. Med. 2015, 13, 7. [CrossRef] [PubMed]
42. Aalami-Harandi, R.; Karamali, M.; Asemi, Z. The favorable e_ects of garlic intake on metabolic profiles, hs-CRP, biomarkers of oxidative stress and pregnancy outcomes in pregnant women at risk for pre-eclampsia: Randomized, double-blind, placebo-controlled trial. J. Matern. Fetal. Neonatal. Med. 2015, 28, 2020–2027.
[CrossRef] [PubMed]
43. Serrano, A.; Ros, G.; Nieto, G. Bioactive compounds and extracts from traditional herbs and their potential anti-inflammatory health e_ects. Medicines 2018, 5, 76. [CrossRef]
44. Zare, E.; Alirezaei, A.; Bakhtiyari, M.; Mansouri, A. Evaluating the e_ect of garlic extract on serum inflammatory markers of peritoneal dialysis patients: A randomized double-blind clinical trial study. BMC Nephrol. 2019, 20, 26. [CrossRef] [PubMed]
45. Kimura, S.; Tung, Y.C.; Pan, M.H.; Su, N.W.; Lai, Y.J.; Cheng, K.C. Black garlic: A critical review of its production, bioactivity, and application. J. Food Drug Anal. 2017, 25, 62–70. [CrossRef] [PubMed]
46. Darooghegi Mofrad, M.; Milajerdi, A.; Koohdani, F.; Surkan, P.J.; Azadbakht, L. Garlic Supplementation Reduces Circulating C-reactive Protein, Tumor Necrosis Factor, and Interleukin-6 in Adults: A Systematic Review and Meta-analysis of Randomized Controlled Trials. J. Nutr. 2019, 149, 605–618. [CrossRef]
47. Percival, S.S. Aged garlic extract modifies human immunity. J. Nutr. 2016, 146, 433S–436S. [CrossRef] [PubMed]
48. Nantz, M.P.; Rowe, C.A.; Muller, C.E.; Creasy, R.A.; Stanilka, J.M.; Percival, S.S. Supplementation with aged garlic extract improves both NK and _-T cell function and reduces the severity of cold and flu symptoms: A randomized, double-blind, placebo-controlled nutrition intervention. Clin. Nutr. 2012, 31, 337–344.
[CrossRef]
49. Xu, C.; Mathews, A.E.; Rodrigues, C.; Eudy, B.J.; Rowe, C.A.; O’Donoughue, A.; Percival, S.S. Aged garlic extract supplementation modifies inflammation and immunity of adults with obesity: A randomized, double-blind, placebo-controlled clinical trial. Clin. Nutr. ESPEN 2018, 24, 148–155. [CrossRef]
50. Ried, K.; Travica, N.; Sali, A. The e_ect of Kyolic aged garlic extract on gut microbiota, inflammation, and cardiovascular markers in hypertensives: The GarGIC Trial. Front. Nutr. 2018, 5, 122. [CrossRef]
51. Van Doorn, M.B.; Santo, S.M.E.; Meijer, P.; Kamerling, I.M.; Schoemaker, R.C.; Dirsch, V.; Vollmar, A.; Ha_ner, T.; Gebhardt, R.; Cohen, A.F.; et al. E_ect of garlic powder on C-reactive protein and plasma lipids in overweight and smoking subjects. Am. J. Clin. Nutr. 2006, 84, 1324–1329. [CrossRef] [PubMed]
52. Warshafsky, S.; Kamer, R.S.; Sivak, S.L. E_ect of garlic on total serum cholesterol: A meta-analysis. Ann. Intern. Med. 1993, 119, 599–605. [CrossRef] [PubMed]
53. Memon, A.R.; Ghanghro, A.B.; Shaikh, I.A.; Qazi, N.; Ghanghro, I.H.; Shaikh, U. E_ects of Olive Oil and Garlic on Serum Cholesterol and Triglycerides Levels in the Patients of Type–II Diabetes Mellitus. J. Liaquat Uni. Med. Health Sci. 2018, 17, 101–105.
54. Silagy, C.A.; Neil, H.A. A meta-analysis of the e_ect of garlic on blood pressure. Europe PMC 1994, 12, 463–468. [CrossRef]
55. Jung, E.S.; Park, S.H.; Choi, E.K.; Ryu, B.H.; Park, B.H.; Kim, D.S.; Kim, Y.G.; Chae, S.W. Reduction of blood lipid parameters by a 12-wk supplementation of aged black garlic: A randomized controlled trial. Nutrition 2014, 30, 1034–1039. [CrossRef]
56. Sobenin, I.A.; Nedosugova, L.V.; Filatova, L.V.; Balabolkin, M.I.; Gorchakova, T.V.; Orekhov, A.N. Metabolic e_ects of time-released garlic powder tablets in type 2 diabetes mellitus: The results of double-blinded placebo-controlled study. Acta Diabetol. 2008, 45, 1–6. [CrossRef]
57. Ashraf, R.; Aamir, K.; Shaikh, A.R.; Ahmed, T. E_ects of garlic on dyslipidemia in patients with type 2 diabetes mellitus. J. Ayub Med. Coll. Abbottabad 2005, 17, 60–64.
58. Turner, B.; Mølgaard, C.; Marckmann, P. E_ect of garlic (Allium sativum) powder tablets on serum lipids, blood pressure and arterial sti_ness in normo-lipidaemic volunteers: A randomised, double-blind, placebo-controlled trial. Br. J. Nutr. 2004, 92, 701–706. [CrossRef]
59. Kojuri, J.; Vosoughi, A.R.; Akrami, M. E_ects of anethum graveolens and garlic on lipid profile in hyperlipidemic patients. Lipids Health Dis. 2007, 6, 5. [CrossRef]
60. Miller, K.D.; Nogueira, L.; Mariotto, A.B.; Rowland, J.H.; Yabro_, K.R.; Alfano, C.M.; Jemal, A.; Kramer, J.L.; Siegel, R.L. Cancer treatment and survivorship statistics. CA Cancer J. Clin. 2019, 69, 363–385. [CrossRef]
61. Rivlin, R.S. Can garlic reduce risk of cancer? Am. J. Clin. Nutr. 2009, 89, 17–18. [CrossRef] [PubMed]
62. Kim, J.Y.; Kwon, O. Garlic intake and cancer risk: An analysis using the Food and Drug Administration’s evidence-based review system for the scientific evaluation of health claims. Am. J. Clin. Nutr. 2008, 89, 257–264. [CrossRef]
63. Zuniga, K.E.; Parma, D.L.; Muñoz, E.; Spaniol, M.;Wargovich, M.; Ramirez, A.G. Dietary intervention among breast cancer survivors increased adherence to a Mediterranean-style, anti-inflammatory dietary pattern: The Rx for Better Breast Health Randomized Controlled Trial. Breast Cancer Res. Treat. 2019, 173, 145–154.
[CrossRef] [PubMed]
64. You, W.C.; Brown, L.M.; Zhang, L.; Li, J.Y.; Jin, M.L.; Chang, Y.S.; Ma, J.L.; Pan, K.F.; Liu, W.D.; Hu, Y.; et al. Randomized double-blind factorial trial of three treatments to reduce the prevalence of precancerous gastric lesions. J. Natl. Cancer Inst. 2006, 98, 974–983. [CrossRef]
65. Li, H.; Li, H.Q.; Wang, Y.; Xu, H.X.; Fan, W.T.; Wang, M.L.; Sun, P.H.; Xie, X.Y. An intervention study to prevent gastric cancer by micro-selenium and large dose of allitridum. Chin. Med. J. 2004, 117, 1155–1160. [PubMed]
66. Ma, J.L.; Zhang, L.; Brown, L.M.; Li, J.Y.; Shen, L.; Pan, K.F.; Liu, W.D.; Hu, Y.; Han, Z.X.; Crystal-Mansour, S.; et al. Fifteen-year e_ects of Helicobacter pylori, garlic, and vitamin treatments on gastriccancer incidence and mortality. J. Natl. Cancer Inst. 2012, 104, 488–492. [CrossRef] [PubMed]
67. Gail, M.H.; You, W.C. A factorial trial including garlic supplements assesses e_ect in reducing precancerous gastric lesions. J. Nutr. 2006, 136, 813S–815S. [CrossRef] [PubMed]
68. Li, W.Q.; Zhang, J.Y.; Ma, J.L.; Li, Z.X.; Zhang, L.; Zhang, Y.; Guo, Y.; Zhou, T.; Li, J.Y.; Shen, L.; et al. E_ects of Helicobacter pylori treatment and vitamin and garlic supplementation on gastric cancer incidence and mortality: Follow-up of a randomized intervention trial. BMJ 2019, 366, l5016. [CrossRef] [PubMed]
69. Wang, Y.; Zhang, L.; Moslehi, R.; Ma, J.; Pan, K.; Zhou, T.; Liu, W.; Brown, L.M.; Hu, Y.; Pee, D.; et al. Long-term garlic or micronutrient supplementation, but not anti-Helicobacter pylori therapy, increases serum folate or glutathione without a_ecting serum vitamin B-12 or homocysteine in a rural Chinese population.J. Nutr. 2008, 139, 106–112. [CrossRef]
70. Dreher, M.L. Dietary Patterns, Whole Plant Foods, Nutrients and Phytochemicals in Colorectal Cancer Prevention and Management. In Dietary Patterns and Whole Plant Foods in Aging and Disease; Humana Press: Cham, Germany, 2018; pp. 521–555.
71. Wu, X.; Shi, J.; Fang, W.X.; Guo, X.Y.; Zhang, L.Y.; Liu, Y.P.; Li, Z. Allium vegetables are associated with reduced risk of colorectal cancer: A hospital-based matched case-control study in China. Asia Pac. J. Clin. Oncol. 2019, 15, e132–e141. [CrossRef]
72. Ngo, S.N.;Williams, D.B.; Cobiac, L.; Head, R.J. Does garlic reduce risk of colorectal cancer? A systematic review. J. Nutr. 2007, 137, 2264–2269. [CrossRef] [PubMed]
73. Ishikawa, H.; Saeki, T.; Otani, T.; Suzuki, T.; Shimozuma, K.; Nishino, H.; Fukuda, S.; Morimoto, K. Aged garlic extract prevents a decline of NK cell number and activity in patients with advanced cancer. J. Nutr. 2006, 136, 816S–820S. [CrossRef] [PubMed]
74. Jin, Z.Y.;Wu, M.; Han, R.Q.; Zhang, X.F.;Wang, X.S.; Liu, A.M.; Zhou, J.Y.; Lu, Q.Y.; Zhang, Z.F.; Zhao, J.K. Raw garlic consumption as a protective factor for lung cancer, a population-based case–control study in a Chinese population. Cancer Prev. Res. 2013, 6, 711–718. [CrossRef]
75. Gatt, M.E.; Strahilevitz, J.; Sharon, N.; Lavie, D.; Goldschmidt, N.; Kalish, Y.; Gural, A.; Paltiel, O.B. A randomized controlled study to determine the e_cacy of garlic compounds in patients with hematological malignancies at risk for chemotherapy-related febrile neutropenia. Integr. Cancer Ther. 2015, 14, 428–435. [CrossRef]
76. Charron, C.S.; Dawson, H.D.; Albaugh, G.P.; Solverson, P.M.; Vinyard, B.T.; Solano-Aguilar, G.I.; Molokin, A.; Novotny, J.A. A single meal containing raw, crushed garlic influences expression of immunity-and cancer-related genes in whole blood of humans. J. Nutr. 2015, 145, 2448–2455. [CrossRef]
77. Smith, S.C.; Collins, A.; Ferrari, R.; Holmes, D.R.; Logstrup, S.; McGhie, D.V.; Ralston, J.; Sacco, R.L.; Stam, H.; Taubert, K.; et al. Our time: A call to save preventable death from cardiovascular disease (heart disease and stroke). J. Am. Coll. Cardiol. 2012, 60, 2343–2348. [CrossRef] [PubMed]
78. Edirisinghe, I.; Banaszewski, K.; Cappozzo, J.; Sandhya, K.; Ellis, C.L.; Tadapaneni, R.; Kappagoda, C.T.; Burton-Freeman, B.M. Strawberry anthocyanin and its association with postprandial inflammation and insulin. Br. J. Nutr. 2011, 106, 913–922. [CrossRef]
79. Zhu, Y.; Anand, R.; Geng, X.; Ding, Y. A mini review: Garlic extract and vascular diseases. Neurol. Res. 2018, 40, 421–425. [CrossRef]
80. Siti, H.N.; Kamisah, Y.; Kamsiah, J. The role of oxidative stress, antioxidants and vascular inflammation in cardiovascular disease (a review). Vasc. Pharmacol. 2015, 71, 40–56. [CrossRef]
81. Leonarduzzi, G.; Gamba, P.; Gargiulo, S.; Biasi, F.; Poli, G. Inflammation-related gene expression by lipid oxidation-derived products in the progression of atherosclerosis. Free Radic. Biol. Med. 2012, 52, 19–34. [CrossRef]
82. Orekhov, A. Direct anti-atherosclerotic therapy; development of natural anti-atherosclerotic drugs preventing cellular cholesterol retention. Curr. Pharm. Des. 2013, 19, 5909–5928. [CrossRef]
83. Sobenin, I.A.; Pryanishnikov, V.V.; Kunnova, L.M.; Rabinovich, Y.A.; Martirosyan, D.M.; Orekhov, A.N. The e_ects of time-released garlic powder tablets on multifunctional cardiovascular risk in patients with coronary artery disease. Lipids Health Dis. 2010, 9, 119. [CrossRef] [PubMed]
84. Zeb, I.; Ahmadi, N.; Flores, F.; Budo_, M.J. Randomized trial evaluating the e_ect of aged garlic extract with supplements versus placebo on adipose tissue surrogates for coronary atherosclerosis progression. Coron. Artery Dis. 2018, 29, 325–328. [CrossRef]
85. Wlosinska, M.; Nilsson, A.C.; Hlebowicz, J.; Malmsjö, M.; Fakhro, M.; Lindstedt, S. Aged garlic extract preserves cutaneous microcirculation in patients with increased risk for cardiovascular diseases: A double-blinded placebo-controlled study. Int. Wound J. 2019, 16, 1487–1493. [CrossRef] [PubMed]
86. Myasoedova, V.A.; Kirichenko, T.V.; Melnichenko, A.A.; Orekhova, V.A.; Ravani, A.; Poggio, P.; Sobenin, I.A.; Bobryshev, Y.V.; Orekhov, A.N. Anti-atherosclerotic e_ects of a phytoestrogen-rich herbal preparation in postmenopausal women. Int. J Mol. Sci. 2016, 17, 1318. [CrossRef] [PubMed]
87. Matsumoto, S.; Nakanishi, R.; Li, D.; Alani, A.; Rezaeian, P.; Prabhu, S.; Abraham, J.; Fahmy, M.A.; Dailing, C.; Flores, F.; et al. Aged garlic extract reduces low attenuation plaque in coronary arteries of patients with metabolic syndrome in a prospective randomized double-blind study. J. Nutr. 2016, 146, 427S–432S. [CrossRef] [PubMed]
88. Sahebkar, A.; Serban, C.; Ursoniu, S.; Banach, M. E_ect of garlic on plasma lipoprotein (a) concentrations: A systematic review and meta-analysis of randomized controlled clinical trials. Nutrition 2016, 32, 33–40. [CrossRef]
89. Mahdavi-Roshan, M.; Mirmiran, P.; Arjmand, M.; Nasrollahzadeh, J. E_ects of garlic on brachial endothelial function and capacity of plasma to mediate cholesterol e_ux in patients with coronary artery disease. Anatol. J. Cardiol. 2017, 18, 116–121. [CrossRef] [PubMed]
90. Zeng, T.; Guo, F.F.; Zhang, C.L.; Song, F.Y.; Zhao, X.L.; Xie, K.Q. A meta-analysis of randomized, double-blind, placebo-controlled trials for the e_ects of garlic on serum lipid profiles. J. Sci. Food Agric. 2012, 92, 1892–1902. [CrossRef]
91. Shafiekhani, M.; Faridi, P.; Kojuri, J.; Namazi, S. Comparison of antiplatelet activity of garlic tablets with cardio-protective dose of aspirin in healthy volunteers: A randomized clinical trial. Avicenna J. Phytomed. 2016, 6, 550–557. [PubMed]
92. Wojcikowski, K.; Myers, S.; Brooks, L. E_ects of garlic oil on platelet aggregation: A double blind placebo controlled crossover study. Platelets 2007, 18, 29–34. [CrossRef]
93. Macan, H.; Uykimpang, R.; Alconcel, M.; Takasu, J.; Razon, R.; Amagase, H.; Niihara, Y. Aged garlic extract may be safe for patients on warfarin therapy. J. Nutr. 2006, 136, 793S–795S. [CrossRef] [PubMed]
94. Samson, S.L.; Garber, A.J. Metabolic syndrome. Endocrinol. Metab. Clinics. 2014, 43, 1–23. [CrossRef] [PubMed]
95. Choudhary, P.R.; Jani, R.D.; Sharma, M.S. E_ect of raw crushed garlic (Allium sativum L.) on components of metabolic syndrome. J. Diet. Suppl. 2018, 15, 499–506. [CrossRef]
96. Varma, M.; Sharma, D.K.; Paaneri, S.; Mishra, A.; Sinha, A.R.S.; Varma, V. Potential clinical benefits of garlic (Allium sativum). J. Environ. Res. Dev. 2011, 5, 652–655.
97. Gomez-Arbelaez, D.; Lahera, V.; Oubiña, P.; Valero-Muñoz, M.; Heras, N.D.L.; Rodríguez, Y.; Garcia, R.G.; Camacho, P.A.; López-Jaramillo, P. Aged garlic extract improves adiponectin levels in subjects with metabolic syndrome: A double-blind, placebo-controlled, randomized, crossover study. Mediat. Inflamm. 2013, 2013, 6. [CrossRef] [PubMed]
98. Magder, S. The meaning of blood pressure. Crit. Care 2018, 22, 257. [CrossRef] [PubMed]
99. Ried, K. Garlic lowers blood pressure in hypertensive individuals, regulates serum cholesterol, and stimulates immunity: An updated meta-analysis and review. J. Nutr. 2016, 146, 389S–396S. [CrossRef] [PubMed]
100. Ried, K.; Frank, O.R.; Stocks, N.P. Aged garlic extract reduces blood pressure in hypertensives: A dose–response trial. Eur. J. Clin. Nutr. 2013, 67, 64–70. [CrossRef] [PubMed]
101. Steiner, M.; Khan, A.H.; Holbert, D.; Lin, R.I. A double-blind crossover study in moderately hypercholesterolemic men that compared the e_ect of aged garlic extract and placebo administration on blood lipids. Am. J. Clin. Nutr. 1996, 64, 866–870. [CrossRef]
102. Ackermann, R.T.; Mulrow, C.D.; Ramirez, G.; Gardner, C.D.; Morbidoni, L.; Lawrence, V.A. Garlic shows promise for improving some cardiovascular risk factors. Arch. Intern. Med. 2001, 161, 813–824. [CrossRef] [PubMed]
103. Nakasone, Y.; Nakamura, Y.; Yamamoto, T.; Yamaguchi, H. E_ect of a traditional Japanese garlic preparation on blood pressure in prehypertensive and mildly hypertensive adults. Exp. Ther. Med. 2013, 5, 399–405. [CrossRef] [PubMed]
104. Zeb, F.; Safdar, M.; Fatima, S.; Khan, S.; Alam, S.; Muhammad, M.; Syed, A.; Habib, F.; Shakoor, H. Supplementation of garlic and coriander seed powder: Impact on body mass index, lipid profile and blood pressure of hyperlipidemic patients. Pak. J. Pharm. Sci. 2018, 31, 1935–1941. [PubMed]
105. Simons, L.A.; Balasubramaniam, S.; Von Konigsmark, M.; Parfitt, A.; Simons, J.; Peters,W. On the e_ect of garlic on plasma lipids and lipoproteins in mild hypercholesterolaemia. Atherosclerosis 1995, 113, 219–225. [CrossRef]
106. Sujithra, K.; Srinivasan, S.; Indumathi, D.; Vinothkumar, V. Allyl methyl sulfide, a garlic active component mitigates hyperglycemia by restoration of circulatory antioxidant status and attenuating glycoprotein components in streptozotocin-induced experimental rats. Toxicol. Mech. Methods 2019, 29, 165–176. [CrossRef] [PubMed]
107. Zheng, Y.; Ley, S.H.; Hu, F.B. Global aetiology and epidemiology of type 2 diabetes mellitus and its complications. Nat. Rev. Endocrinol. 2018, 14, 88–98. [CrossRef] [PubMed]
108. Herman, W.H. The global burden of diabetes: An overview. In Diabetes Mellitus in Developing Countries and Underserved Communities; Springer: Cham, Germany, 2017; pp. 1–5.
109. Melino, S.; Leo, S.; Toska Papajani, V. Natural Hydrogen Sulfide Donors from Allium sp. as a Nutraceutical Approach in Type 2 Diabetes Prevention and Therapy. Nutrition 2019, 11, 1581. [CrossRef] [PubMed]
110. Shabani, E.; Sayemiri, K.; Mohammadpour, M. The e_ect of garlic on lipid profile and glucose parameters in diabetic patients: A systematic review and meta-analysis. Prim. Care Diabetes 2019, 13, 28–42. [CrossRef]
111. Hou, L.Q.; Liu, Y.H.; Zhang, Y.Y. Garlic intake lowers fasting blood glucose: Meta-analysis of randomized controlled trials. Asia Pac. J. Clin. Nutr. 2015, 24, 575–582.
112. Phil, R.A.; Khan, R.A.; Ashraf, I. E_ects of garlic on blood glucose levels and HbA1c in patients with type 2 diabetes mellitus. J. Med. Plant Res. 2011, 5, 2922–2928.
113. Ghorbani, A.; Zarvandi, M.; Rakhshandeh, H. A Randomized Controlled Trial of a Herbal Compound for Improving Metabolic Parameters in Diabetic Patients with Uncontrolled Dyslipidemia. Endocr. Metab. Immune Disord. Drug Targets 2019, 19, 1075–1082. [CrossRef]
114. Ashraf, R.; Khan, R.A.; Ashraf, I. Garlic (Allium sativum) supplementation with standard antidiabetic agent provides better diabetic control in type 2 diabetes patients. Pak. J. Pharm. Sci. 2011, 24, 565–570.
115. Parham, M.; Bagherzadeh, M.; Asghari, M.; Akbari, H.; Hosseini, Z.; Rafiee, M.; Vafaeimanesh, J. Evaluating the e_ect of a herb on the control of blood glucose and insulin-resistance in patients with advanced type 2 diabetes (a double-blind clinical trial). Caspian J. Intern. Med. 2020, 11, 12–20. [PubMed]
116. Dehghani, S.; Alipoor, E.; Salimzadeh, A.; Yaseri, M.; Hosseini, M.; Feinle-Bisset, C.; Hosseinzadeh-Attar, M.J. The e_ect of a garlic supplement on the pro-inflammatory adipocytokines, resistin and tumor necrosis factor-alpha, and on pain severity, in overweight or obese women with knee osteoarthritis. Phytomedicine 2018, 48, 70–75. [CrossRef] [PubMed]
117. Salimzadeh, A.; Alipoor, E.; Dehghani, S.; Yaseri, M.; Hosseini, M.; Feinle-Bisset, C.; Hosseinzadeh-Attar, M.J. The e_ect of 12-week garlic supplementation on symptom relief in overweight or obese women with knee osteoarthritis. Int. J. Clin. Pract. Suppl. 2018, 72, e13208. [CrossRef] [PubMed]
118. Moza_ari-Khosravi, H.; Hesabgar, H.A.S.; Owlia, M.B.; Hadinedoushan, H.; Barzegar, K.; Fllahzadeh, M.H. The e_ect of garlic tablet on pro-inflammatory cytokines in postmenopausal osteoporotic women: A randomized controlled clinical trial. J. Diet. Suppl. 2012, 9, 262–271. [CrossRef] [PubMed]
119. Feily, A.; Namazi, M.R.; Pazyar, N.; Saboktakin, M.; Saboktakin, M. Garlic extract as a novel addition to antikeloid armamentarium: An untested hypothesis. J. Altern. Complement. Med. 2009, 15, 1153–1154. [CrossRef]
120. Kenawy, S.; Mohammed, G.F.; Younes, S.; Elakhras, A.I. Evaluation of TNF-_ serum level in patients with recalcitrant multiple common warts, treated by lipid garlic extract. Dermatol. Ther. 2014, 27, 272–277. [CrossRef]
121. Bakhshi, M.; Taheri, J.B.; Basir Shabestari, S.; Tanik, A.; Pahlevan, R. Comparison of therapeutic e_ect of aqueous extract of garlic and nystatin mouthwash in denture stomatitis. Gerodontology 2012, 29, e680–e684. [CrossRef]
122. Kundakovi´c, T.; Milenkovi´c, M.; Zlatkovi´c, S.; Nikoli´c, V.; Nikoli´c, G.; Bini´c, I. Treatment of venous ulcers with the herbal-based ointment Herbadermal®: A prospective non-randomized pilot study. Res. Complementary Med. 2012, 19, 26–30. [CrossRef]
123. Ejaz, S.; Chekarova, I.; Cho, J.W.; Lee, S.Y.; Ashraf, S.; Lim, C.W. E_ect of aged garlic extract on wound healing: A new frontier in wound management. Drug Chem. Toxicol. 2009, 32, 191–203. [CrossRef] [PubMed]
124. Ranjani, M.; Rajan, S.; Brindha, P. Antioxidant and antibacterial potentials of Aloe vera juice extract against wound isolates. J. Pure Appl. Microbiol. 2010, 4, 733–739.
125. Johnson, S.M.; Horn, T.D. Intralesional immunotherapy for warts using a combination of skin test antigens: A safe and e_ective therapy. J. Drugs Dermatol. JDD 2004, 3, 263–265. [PubMed]
126. Kus, S.; Ergun, T.; Gun, D.; Akin, O. Intralesional tuberculin for treatment of refractory warts. J. Eur. Acad. Dermatol. Venereol. 2005, 19, 515–516. [CrossRef] [PubMed]
127. Horn, T.D.; Johnson, S.M.; Helm, R.M.; Roberson, P.K. Intralesional immunotherapy of warts with mumps, Candida, and Trichophyton skin test antigens: A single-blinded, randomized, and controlled trial. Arch. Dermatol. 2005, 141, 589–594. [CrossRef] [PubMed]
128. Gökalp, F. The inhibition e_ect of garlic-derived compounds on human immunodeficiency virus type 1 and saquinavir. J. Biochem. Mol. Toxicol. 2018, 32, e22215. [CrossRef]
129. Serrano Gruhlke, H.D.A.; Mariezcurrena-Berasain, M.A.; Castillo, A.D.C.G.; Carranza, B.V.; Pliego, A.B.; Rojas, M.T.; Anele, U.Y.; Salem, A.Z.M.; Rivas-Caceres, R.R. Antimicrobial resistance of three common molecularly identified pathogenic bacteria to Allium aqueous extracts. Microb. Pathog. 2020, 142, 104028. [CrossRef]
130. Gruhlke, M.C.H.; Portz, D.; Stitz, M.; Anwar, A.; Schneider, T.; Jacob, C.; Schlaich, N.L.; Slusarenko, A.J. Allicin disrupts the cell’s electrochemical potential and induces apoptosis in yeast. Free Radic. Biol. Med. 2010, 49, 1916–1924. [CrossRef]
131. Said, M.M.;Watson, C.; Grando, D. Garlic alters the expression of putative virulence factor genes SIR2 and ECE1 in vulvovaginal C. albicans isolates. Sci. Rep. 2020, 10, 1–9. [CrossRef]
132. Gao, X.; Chen, Y.; Chen, Z.; Xue, Z.; Jia, Y.; Guo, Q.; Ma, Q.; Zhang, M.; Chen, H. Identification and antimicrobial activity evaluation of three peptides from laba garlic and the related mechanism. Food Funct. 2019, 10, 4486–4496. [CrossRef]
133. Thomas, A.; Thakur, S.; Habib, R. Comparison of antimicrobial e_cacy of green tea, garlic with lime, and sodium fluoride mouth rinses against Streptococcus mutans, Lactobacilli species, and Candida albicans in children: A randomized double-blind controlled clinical trial. Int. J. Clin. Pediatr. Dent. 2017, 10, 234–239. [PubMed]
134. Ebrahimy, F.; Dolatian, M.; Moatar, F.; Majd, H.A. Comparison of the therapeutic e_ects of Garcin® and fluconazole on Candida vaginitis. Singap. Med. J. 2015, 56, 567. [CrossRef] [PubMed]
135. Watson, C.J.; Grando, D.; Fairley, C.K.; Chondros, P.; Garland, S.M.; Myers, S.P.; Pirotta, M. The effects of oral garlic on vaginal candida colony counts: A randomised placebo controlled double-blind trial. BJOG 2014, 121, 498–506. [CrossRef]
136. Andrianova, I.V.; Sobenin, I.A.; Sereda, E.V.; Borodina, L.I.; Studenikin, M.I. E_ect of long-acting garlic tablets “allicor” on the incidence of acute respiratory viral infections in children. Ter. Arkhiv 2003, 75, 53–56.
137. Madineh, H.; Yadollahi, F.; Yadollahi, F.; Mofrad, E.P.; Kabiri, M. Impact of garlic tablets on nosocomial infections in hospitalized patients in intensive care units. Electron. Physician 2017, 9, 4064–4071. [CrossRef] [PubMed]
138. Foroutan-Rad, M.; Tappeh, K.H.; Khademvatan, S. Antileishmanial and Immunomodulatory Activity of Allium sativum (Garlic) A Review. J. Evid. Based Complement. Alternat. Med. 2017, 22, 141–155. [CrossRef]
139. Samdani, A.J.; Iqbal Choudhary, M. Laboratory studies and clinical trials on new formulations from garlic extract against cutaneous leishmaniasis. Anti-Infect. Agents 2012, 10, 111–116. [CrossRef]
140. Smyth, A.R.; Cifelli, P.M.; Ortori, C.A.; Righetti, K.; Lewis, S.; Erskine, P.; Holland, E.D.; Givskov, M.; Williams, P.; Cámara, M.; et al. Garlic as an inhibitor of Pseudomonas aeruginosa quorum sensing in cystic fibrosis—A pilot randomized controlled trial. Pediatr. Pulmonol. 2010, 45, 356–362.
141. Kim, H.N.; Kang, S.G.; Roh, Y.K.; Choi, M.K.; Song, S.W. E_cacy and safety of fermented garlic extract on hepatic function in adults with elevated serum gamma-glutamyl transpeptidase levels: A double-blind, randomized, placebo-controlled trial. Eur. J. Nutr. 2017, 56, 1993–2002. [CrossRef]
142. Panjeshahin, A.; Mollahosseini, M.; Panbehkar-Jouybari, M.; Kaviani, M.; Mirzavandi, F.; Hosseinzadeh, M. Effects of garlic supplementation on liver enzymes: A systematic review and meta-analysis of randomized controlled trials. Phytother. Res. 2020. [CrossRef]
143. Lee, M.H.; Kim, Y.M.; Kim, S.G. E_cacy and tolerability of diphenyl-dimethyl-dicarboxylate plus garlic oil in patients with chronic hepatitis. Int. J. Clin. Pharm. Ther. 2012, 50, 778–786. [CrossRef] [PubMed]
144. Soleimani, D.; Paknahad, Z.; Askari, G.; Iraj, B.; Feizi, A. E_ect of garlic powder consumption on body composition in patients with nonalcoholic fatty liver disease: Arandomized, double-blind, placebo-controlled trial. Adv. Biomed. Res. 2016, 5, 2. [CrossRef] [PubMed]
145. Zhang, S.; Gu, Y.;Wang, L.; Zhang, Q.; Liu, L.; Lu, M.; Meng, G.; Yao, Z.;Wu, H.; Xia, Y.; et al. Association between dietary raw garlic intake and newly diagnosed nonalcoholic fatty liver disease: A population-based study. Eur. J. Endocrinol. 2019, 181, 591–602. [CrossRef] [PubMed]
© 2020 by the authors. Licensee MDPI, Basel, Switzerland. This article is an open access article distributed under the terms and conditions of the Creative Commons Attribution (CC BY) license (http://creativecommons.org/licenses/by/4.0/).
Jiaojiao Zhang 1, Maria Elexpuru-Zabaleta 4 , Jesus Simal-Gandara 5 ,
Francesca Giampieri 1,2,6,* and Maurizio Battino 1,2,7,*1 Dipartimento di Scienze Cliniche Specialistiche e Odontostomtologiche—Università Politecnica delle
Marche, Via Ranieri 65, 60130 Ancona, Italy; j.ansary@pm.univpm.it (J.A.); d.cianciosi@pm.univpm.it (D.C.);
j.zhang@pm.univpm.it (J.Z.)
2 Nutrition and Food Science Group, department of Analytical and Food Chemistry, CITACA, CACTI,
University of Vigo-Vigo Campus, 36310 Vigo, Spain; tforbes@uvigo.es
3 Nutrition and Food Science Group, Department of Biochemistry, Genetics and Immunology,
Faculty of Biology, University of Vigo, 36310 Vigo, Spain; egil@uvigo.es
4 Dipartimento di Scienze Cliniche e Molecolari, Facoltà di Medicina, Università Politecnica delle Marche,
60131 Ancona, Italy; p015008@sta_.univpm.it
5 Nutrition and Bromatology Group, Department of Analytical and Food Chemistry, Faculty of Science,
University of Vigo, Ourense Campus, E-32004 Ourense, Spain; jsimal@uvigo.es
6 College of Food Science and Technology, Northwest University, Xi’an, Shaanxi 710069, China
7 International Research Center for Food Nutrition and Safety, Jiangsu University, Zhenjiang 212013, China
Эти авторы внесли равный вкладВклад авторов: концептуализация – J.A и T.Y.F.-H; написание – подготовка финального варианта J.A и T.Y.F.-H и D.C.; цифры и таблицы – J.Z. и M.E.-Z; написание – правки и рецензирование – E.G. и J.S. -G; контроль – M.B. Все авторы прочитали и согласны с опубликованным материалом. Бюджет: без внешнего финансирования. Благодарности: T.Y.F.-H работает с «Juan de la Cierva-Formacio`n» (постдокторантурный контракт). Конфликт интересов: авторы не сообщают о конфликте интересов. Список литературы1. Jiang, T.A. Health Benefits of Culinary Herbs and Spices. J. AOAC Int. 2019, 102, 395–411. [CrossRef] [PubMed]
2. Petrovska, B.B.; Cekovska, S. Extracts from the history and medical properties of garlic. Pharmacogn. Rev. 2010, 4, 106–110. [CrossRef] [PubMed]
3. Setiawan, V.W.; Yu, G.P.; Lu, Q.Y.; Lu, M.L.; Yu, S.Z.; Mu, L.; Zhang, J.G.; Kurtz, R.C.; Cai, L.; Hsieh, C.C.; et al. Allium vegetables and stomach cancer risk in China. Asian Pac. J. Cancer Prev. APJCP 2005, 6, 387–395.
4. Diretto, G.; Rubio-Moraga, A.; Argandoña, J.; Castillo, P.; Gómez-Gómez, L.; Ahrazem, O. Tissue-specific accumulation of sulfur compounds and saponins in different parts of garlic cloves from purple and white ecotypes. Molecules 2017, 22, 1359. [CrossRef] [PubMed]
5. Gorinstein, S.; Leontowicz, H.; Leontowicz, M.; Namiesnik, J.; Najman, K.; Drzewiecki, J.; Cvikrová, M.; Martincová, O.; Katrich, E.; Trakhtenberg, S. Comparison of the main bioactive compounds and antioxidant activities in garlic and white and red onions after treatment protocols. J. Agric. Food Chem. 2008, 56, 4418–4426.
[CrossRef] [PubMed]
6. Wang, Y.; Guan, M.; Zhao, X.; Li, X. Effects of garlic polysaccharide on alcoholic liver fibrosis and intestinal microflora in mice. Pharm. Biol. 2018, 56, 325–332. [CrossRef]
7. Liang, J.J.; Li, H.R.; Chen, Y.; Zhang, C.; Chen, D.G.; Liang, Z.C.; Shi, Y.Q.; Zhang, L.L.; Xin, L.; Zhao, D.B. Diallyl Trisulfide can induce fibroblast-like synovial apoptosis and has a therapeutic effect on collagen-induced arthritis in mice via blocking NF-B and Wnt pathways. Int. Immunopharmacol. 2019, 71, 132–138. [CrossRef]
8. Jiang, X.Y.; Zhu, X.S.; Xu, H.Y.; Zhao, Z.X.; Li, S.Y.; Li, S.Z.; Cai, J.H.; Cao, J.M. Diallyl trisulfide suppresses tumor growth through the attenuation of Nrf2/Akt and activation of p38/JNK and potentiates cisplatin efficacy in gastric cancer treatment. Acta Pharmacol. Sin. 2017, 38, 1048–1058. [CrossRef]
9. Lv, Y.; So, K.-F.; Wong, N.-K.; Xiao, J. Anti-cancer activities of S-allylmercaptocysteine from aged garlic. Chin. J. Nat. Med. 2019, 17, 43–49. [CrossRef]
10. Ohtani, M.; Nishimura, T. Sulfur-containing amino acids in aged garlic extract inhibit inflammation in human gingival epithelial cells by suppressing intercellular adhesion molecule-1 expression and IL-6 secretion. Biomed. Rep. 2020, 12, 99–108. [CrossRef]
11. Kiesel, V.A.; Stan, S.D. Diallyl trisulfide, a chemopreventive agent from Allium vegetables, inhibits alpha-secretases in breast cancer cells. Biochem. Biophys. Res. Commun. 2017, 484, 833–838. [CrossRef]
12. Lu, J.; Cheng, B.; Meng, Z.; Fang, B.; Li, T.; Sun, M.; Liu, M.; Guan, S. Alliin attenuates 1, 3-dichloro-2-propanol-induced lipogenesis in HepG2 cells through activation of the AMP-activated protein
kinase-dependent pathway. Life Sci. 2018, 195, 19–24. [CrossRef]
13. Wang, M.J.; Cai, W.J.; Zhu, Y.C. Mechanisms of angiogenesis: Role of hydrogen sulphide. Clin. Exp. Pharmacol. Physiol. 2010, 37, 764–771. [CrossRef]
14. Kong, F.; Lee, B.H.;Wei, K. 5-Hydroxymethylfurfural Mitigates Lipopolysaccharide-Stimulated Inflammation via Suppression of MAPK, NF-B and mTOR Activation in RAW 264.7 Cells. Molecules 2019, 24, 275. [CrossRef] [PubMed]
15. Padiya, R.; Chowdhury, D.; Borkar, R.; Srinivas, R.; Bhadra, M.P.; Banerjee, S.K. Garlic attenuates cardiac oxidative stress via activation of PI3K/AKT/Nrf2-Keap1 pathway in fructose-fed diabetic rat. PLoS ONE 2014, 9, e94228. [CrossRef] [PubMed]
16. Alma, E.; Eken, A.; Ercil, H.; Yelsel, K.; Daglioglu, N. The effect of garlic powder on human urinary cytokine excretion. Urol. J. 2014, 11, 1308–1315.
17. Lawson, L.D.; Gardner, C.D. Composition, stability, and bioavailability of garlic products used in a clinical trial. J. Agric. Food Chem. 2005, 53, 6254–6261. [CrossRef]
18. Agarwal, K.C. Therapeutic actions of garlic constituents. Med. Res. Rev. 1996, 16, 111–124. [CrossRef]
19. Gu, C.; Howell, K.; Dunshea, F.R.; Suleria, H.A. Lc-esi-qtof/ms characterisation of phenolic acids and flavonoids in polyphenol-rich fruits and vegetables and their potential antioxidant activities. Antioxidants 2019, 8, 405. [CrossRef] [PubMed]
20. Dziri, S.; Hassen, I.; Fatnassi, S.; Mrabet, Y.; Casabianca, H.; Hanchi, B.; Hosni, K. Phenolic constituents, antioxidant and antimicrobial activities of rosy garlic (Allium roseum var. odoratissimum). J. Funct. Foods 2012, 4, 423–432. [CrossRef]
21. Fenwick, G.R.; Hanley, A.B.; Whitaker, J.R. The genus allium. Part 2. Crit. Rev. Food Sci. Nutr. 1985, 22, 273–377. [CrossRef] [PubMed]
22. Londhe, V.P. Role of garlic (Allium sativum) in various diseases: An overview. Angiogenesis 2011, 12, 13.
23. Rana, S.V.; Pal, R.; Vaiphei, K.; Sharma, S.K.; Ola, R.P. Garlic in health and disease. Nutr. Res. Rev. 2011, 24, 60–71. [CrossRef] [PubMed]
24. Lawson, L.D.; Hunsaker, S.M. Allicin bioavailability and bioequivalence from garlic supplements and garlic foods. Nutrients 2018, 10, 812. [CrossRef]
25. Lawson, L.D.; Ransom, D.K.; Hughes, B.G. Inhibition of whole blood platelet-aggregation by compounds in garlic clove extracts and commercial garlic products. Thromb. Res. 1992, 65, 141–156. [CrossRef]
26. Freeman, F.; Kodera, Y. Garlic chemistry: Stability of S-(2-propenyl)-2-propene-1-sulfinothioate (allicin) in blood, solvents, and simulated physiological fluids. J. Agric. Food Chem. 1995, 43, 2332–2338. [CrossRef]
27. Germain, E.; Auger, J.; Ginies, C.; Siess, M.H.; Teyssier, C. In vivo metabolism of diallyl disulphide in the rat: Identification of two new metabolites. Xenobiotica 2002, 32, 1127–1138. [CrossRef]
28. Nagae, S.; Ushijima, M.; Hatono, S.; Imai, J.; Kasuga, S.; Matsuura, H.; Itakura, Y.; Higashi, Y. Pharmacokinetics of the garlic compound S-allylcysteine. Planta Med. 1994, 60, 214–217. [CrossRef]
29. Berginc, K.; Milisav, I.; Kristl, A. Garlic flavonoids and organosulfur compounds: Impact on the hepatic pharmacokinetics of saquinavir and darunavir. Drug Metab. Pharmacokinet. 2010, 25, 521–530. [CrossRef]
30. Miraghajani, M.; Rafie, N.; Hajianfar, H.; Larijani, B.; Azadbakht, L. Aged garlic and cancer: A systematic review. Int. J. Prev. Med. 2018, 9, 84.
31. Petropoulos, S.; Fernandes, Â.; Barros, L.; Ciric, A.; Sokovic, M.; Ferreira, I.C. Antimicrobial and antioxidant properties of various Greek garlic genotypes. Food Chem. 2018, 245, 7–12. [CrossRef] [PubMed]
32. Tsuneyoshi, T. BACH1 mediates the antioxidant properties of aged garlic extract. Exp. Ther. Med. 2020, 1500–1503. [CrossRef]
33. Szulin´ ska, M.; Kre˛gielska-Naroz˙na, M.; S´wia˛tek, J.; Stys´, P.; Kuz´nar-Kamin´ ska, B.; Jakubowski, H.; Walkowiak, J.; Bogda´ nski, P. Garlic extract favorably modifies markers of endothelial function in obese patients–randomized double blind placebo-controlled nutritional intervention. Biomed. Pharmacother. 2018, 102, 792–797. [CrossRef]
34. Mirunalini, S.; Krishnaveni, M.; Ambily, V. E effects of raw garlic (Allium sativum) on hyperglycemia in patients with type 2 diabetes mellitus. Pharmacologyonline 2011, 2, 968–974.
35. Moosavian, S.P.; Arab, A.; Paknahad, Z.; Moradi, S. The effects of garlic supplementation on oxidative stress markers: A systematic review and meta-analysis of randomized controlled trials. Complement. Ther. Med. 2020, 50, 102385. [CrossRef] [PubMed]
36. Ahmadian, F.; Moza ari-Khosravi, H.; Azaraein, M.H.; Faraji, R.; Zavar-Reza, J. The effect of consumption of garlic tablet on proteins oxidation biomarkers in postmenopausal osteoporotic women: A randomized clinical trial. Electron. Physician 2017, 9, 5670–5675. [CrossRef] [PubMed]
37. Khoobkhahi, N.; Delavar, R.; Nayebifar, S.H. The combinatory effects of combined training (endurance–resistance) and garlic supplementation on oxidative stress and antioxidant adaptations in untrained boys. Sci. Sports 2019, 34, 410.e1–410.e7. [CrossRef]
38. Atkin, M.; Laight, D.; Cummings, M.H. The effects of garlic extract upon endothelial function, vascular inflammation, oxidative stress and insulin resistance in adults with type 2 diabetes at high cardiovascular risk. A pilot double blind randomized placebo controlled trial. J. Diabetes Complicat 2016, 30, 723–727. [CrossRef]
39. Williams, M.J.; Sutherland,W.H.; McCormick, M.P.; Yeoman, D.J.; De Jong, S.A. Aged garlic extract improves endothelial function in men with coronary artery disease. Phytother. Res. 2005, 19, 314–319. [CrossRef]
40. Lee, G.Y.; Lee, J.J.; Lee, S.M. Antioxidant and anticoagulant status were improved by personalized dietary intervention based on biochemical and clinical parameters in cancer patients. Nutr. Cancer 2015, 67, 1083–1092. [CrossRef] McCrea, C.E.; West, S.G.; Kris-Etherton, P.M.; Lambert, J.D.; Gaugler, T.L.; Teeter, D.L.; Sauder, K.A.; Gu, Y.; Glisan, S.L.; Skulas-Ray, A.C. E_ects of culinary spices and psychological stress on postprandial lipemia and lipase activity: Results of a randomized crossover study and in vitro experiments. J. Transl. Med. 2015, 13, 7. [CrossRef] [PubMed]
42. Aalami-Harandi, R.; Karamali, M.; Asemi, Z. The favorable e_ects of garlic intake on metabolic profiles, hs-CRP, biomarkers of oxidative stress and pregnancy outcomes in pregnant women at risk for pre-eclampsia: Randomized, double-blind, placebo-controlled trial. J. Matern. Fetal. Neonatal. Med. 2015, 28, 2020–2027.
[CrossRef] [PubMed]
43. Serrano, A.; Ros, G.; Nieto, G. Bioactive compounds and extracts from traditional herbs and their potential anti-inflammatory health e_ects. Medicines 2018, 5, 76. [CrossRef]
44. Zare, E.; Alirezaei, A.; Bakhtiyari, M.; Mansouri, A. Evaluating the e_ect of garlic extract on serum inflammatory markers of peritoneal dialysis patients: A randomized double-blind clinical trial study. BMC Nephrol. 2019, 20, 26. [CrossRef] [PubMed]
45. Kimura, S.; Tung, Y.C.; Pan, M.H.; Su, N.W.; Lai, Y.J.; Cheng, K.C. Black garlic: A critical review of its production, bioactivity, and application. J. Food Drug Anal. 2017, 25, 62–70. [CrossRef] [PubMed]
46. Darooghegi Mofrad, M.; Milajerdi, A.; Koohdani, F.; Surkan, P.J.; Azadbakht, L. Garlic Supplementation Reduces Circulating C-reactive Protein, Tumor Necrosis Factor, and Interleukin-6 in Adults: A Systematic Review and Meta-analysis of Randomized Controlled Trials. J. Nutr. 2019, 149, 605–618. [CrossRef]
47. Percival, S.S. Aged garlic extract modifies human immunity. J. Nutr. 2016, 146, 433S–436S. [CrossRef] [PubMed]
48. Nantz, M.P.; Rowe, C.A.; Muller, C.E.; Creasy, R.A.; Stanilka, J.M.; Percival, S.S. Supplementation with aged garlic extract improves both NK and _-T cell function and reduces the severity of cold and flu symptoms: A randomized, double-blind, placebo-controlled nutrition intervention. Clin. Nutr. 2012, 31, 337–344.
[CrossRef]
49. Xu, C.; Mathews, A.E.; Rodrigues, C.; Eudy, B.J.; Rowe, C.A.; O’Donoughue, A.; Percival, S.S. Aged garlic extract supplementation modifies inflammation and immunity of adults with obesity: A randomized, double-blind, placebo-controlled clinical trial. Clin. Nutr. ESPEN 2018, 24, 148–155. [CrossRef]
50. Ried, K.; Travica, N.; Sali, A. The e_ect of Kyolic aged garlic extract on gut microbiota, inflammation, and cardiovascular markers in hypertensives: The GarGIC Trial. Front. Nutr. 2018, 5, 122. [CrossRef]
51. Van Doorn, M.B.; Santo, S.M.E.; Meijer, P.; Kamerling, I.M.; Schoemaker, R.C.; Dirsch, V.; Vollmar, A.; Ha_ner, T.; Gebhardt, R.; Cohen, A.F.; et al. E_ect of garlic powder on C-reactive protein and plasma lipids in overweight and smoking subjects. Am. J. Clin. Nutr. 2006, 84, 1324–1329. [CrossRef] [PubMed]
52. Warshafsky, S.; Kamer, R.S.; Sivak, S.L. E_ect of garlic on total serum cholesterol: A meta-analysis. Ann. Intern. Med. 1993, 119, 599–605. [CrossRef] [PubMed]
53. Memon, A.R.; Ghanghro, A.B.; Shaikh, I.A.; Qazi, N.; Ghanghro, I.H.; Shaikh, U. E_ects of Olive Oil and Garlic on Serum Cholesterol and Triglycerides Levels in the Patients of Type–II Diabetes Mellitus. J. Liaquat Uni. Med. Health Sci. 2018, 17, 101–105.
54. Silagy, C.A.; Neil, H.A. A meta-analysis of the e_ect of garlic on blood pressure. Europe PMC 1994, 12, 463–468. [CrossRef]
55. Jung, E.S.; Park, S.H.; Choi, E.K.; Ryu, B.H.; Park, B.H.; Kim, D.S.; Kim, Y.G.; Chae, S.W. Reduction of blood lipid parameters by a 12-wk supplementation of aged black garlic: A randomized controlled trial. Nutrition 2014, 30, 1034–1039. [CrossRef]
56. Sobenin, I.A.; Nedosugova, L.V.; Filatova, L.V.; Balabolkin, M.I.; Gorchakova, T.V.; Orekhov, A.N. Metabolic e_ects of time-released garlic powder tablets in type 2 diabetes mellitus: The results of double-blinded placebo-controlled study. Acta Diabetol. 2008, 45, 1–6. [CrossRef]
57. Ashraf, R.; Aamir, K.; Shaikh, A.R.; Ahmed, T. E_ects of garlic on dyslipidemia in patients with type 2 diabetes mellitus. J. Ayub Med. Coll. Abbottabad 2005, 17, 60–64.
58. Turner, B.; Mølgaard, C.; Marckmann, P. E_ect of garlic (Allium sativum) powder tablets on serum lipids, blood pressure and arterial sti_ness in normo-lipidaemic volunteers: A randomised, double-blind, placebo-controlled trial. Br. J. Nutr. 2004, 92, 701–706. [CrossRef]
59. Kojuri, J.; Vosoughi, A.R.; Akrami, M. E_ects of anethum graveolens and garlic on lipid profile in hyperlipidemic patients. Lipids Health Dis. 2007, 6, 5. [CrossRef]
60. Miller, K.D.; Nogueira, L.; Mariotto, A.B.; Rowland, J.H.; Yabro_, K.R.; Alfano, C.M.; Jemal, A.; Kramer, J.L.; Siegel, R.L. Cancer treatment and survivorship statistics. CA Cancer J. Clin. 2019, 69, 363–385. [CrossRef]
61. Rivlin, R.S. Can garlic reduce risk of cancer? Am. J. Clin. Nutr. 2009, 89, 17–18. [CrossRef] [PubMed]
62. Kim, J.Y.; Kwon, O. Garlic intake and cancer risk: An analysis using the Food and Drug Administration’s evidence-based review system for the scientific evaluation of health claims. Am. J. Clin. Nutr. 2008, 89, 257–264. [CrossRef]
63. Zuniga, K.E.; Parma, D.L.; Muñoz, E.; Spaniol, M.;Wargovich, M.; Ramirez, A.G. Dietary intervention among breast cancer survivors increased adherence to a Mediterranean-style, anti-inflammatory dietary pattern: The Rx for Better Breast Health Randomized Controlled Trial. Breast Cancer Res. Treat. 2019, 173, 145–154.
[CrossRef] [PubMed]
64. You, W.C.; Brown, L.M.; Zhang, L.; Li, J.Y.; Jin, M.L.; Chang, Y.S.; Ma, J.L.; Pan, K.F.; Liu, W.D.; Hu, Y.; et al. Randomized double-blind factorial trial of three treatments to reduce the prevalence of precancerous gastric lesions. J. Natl. Cancer Inst. 2006, 98, 974–983. [CrossRef]
65. Li, H.; Li, H.Q.; Wang, Y.; Xu, H.X.; Fan, W.T.; Wang, M.L.; Sun, P.H.; Xie, X.Y. An intervention study to prevent gastric cancer by micro-selenium and large dose of allitridum. Chin. Med. J. 2004, 117, 1155–1160. [PubMed]
66. Ma, J.L.; Zhang, L.; Brown, L.M.; Li, J.Y.; Shen, L.; Pan, K.F.; Liu, W.D.; Hu, Y.; Han, Z.X.; Crystal-Mansour, S.; et al. Fifteen-year e_ects of Helicobacter pylori, garlic, and vitamin treatments on gastriccancer incidence and mortality. J. Natl. Cancer Inst. 2012, 104, 488–492. [CrossRef] [PubMed]
67. Gail, M.H.; You, W.C. A factorial trial including garlic supplements assesses e_ect in reducing precancerous gastric lesions. J. Nutr. 2006, 136, 813S–815S. [CrossRef] [PubMed]
68. Li, W.Q.; Zhang, J.Y.; Ma, J.L.; Li, Z.X.; Zhang, L.; Zhang, Y.; Guo, Y.; Zhou, T.; Li, J.Y.; Shen, L.; et al. E_ects of Helicobacter pylori treatment and vitamin and garlic supplementation on gastric cancer incidence and mortality: Follow-up of a randomized intervention trial. BMJ 2019, 366, l5016. [CrossRef] [PubMed]
69. Wang, Y.; Zhang, L.; Moslehi, R.; Ma, J.; Pan, K.; Zhou, T.; Liu, W.; Brown, L.M.; Hu, Y.; Pee, D.; et al. Long-term garlic or micronutrient supplementation, but not anti-Helicobacter pylori therapy, increases serum folate or glutathione without a_ecting serum vitamin B-12 or homocysteine in a rural Chinese population.J. Nutr. 2008, 139, 106–112. [CrossRef]
70. Dreher, M.L. Dietary Patterns, Whole Plant Foods, Nutrients and Phytochemicals in Colorectal Cancer Prevention and Management. In Dietary Patterns and Whole Plant Foods in Aging and Disease; Humana Press: Cham, Germany, 2018; pp. 521–555.
71. Wu, X.; Shi, J.; Fang, W.X.; Guo, X.Y.; Zhang, L.Y.; Liu, Y.P.; Li, Z. Allium vegetables are associated with reduced risk of colorectal cancer: A hospital-based matched case-control study in China. Asia Pac. J. Clin. Oncol. 2019, 15, e132–e141. [CrossRef]
72. Ngo, S.N.;Williams, D.B.; Cobiac, L.; Head, R.J. Does garlic reduce risk of colorectal cancer? A systematic review. J. Nutr. 2007, 137, 2264–2269. [CrossRef] [PubMed]
73. Ishikawa, H.; Saeki, T.; Otani, T.; Suzuki, T.; Shimozuma, K.; Nishino, H.; Fukuda, S.; Morimoto, K. Aged garlic extract prevents a decline of NK cell number and activity in patients with advanced cancer. J. Nutr. 2006, 136, 816S–820S. [CrossRef] [PubMed]
74. Jin, Z.Y.;Wu, M.; Han, R.Q.; Zhang, X.F.;Wang, X.S.; Liu, A.M.; Zhou, J.Y.; Lu, Q.Y.; Zhang, Z.F.; Zhao, J.K. Raw garlic consumption as a protective factor for lung cancer, a population-based case–control study in a Chinese population. Cancer Prev. Res. 2013, 6, 711–718. [CrossRef]
75. Gatt, M.E.; Strahilevitz, J.; Sharon, N.; Lavie, D.; Goldschmidt, N.; Kalish, Y.; Gural, A.; Paltiel, O.B. A randomized controlled study to determine the e_cacy of garlic compounds in patients with hematological malignancies at risk for chemotherapy-related febrile neutropenia. Integr. Cancer Ther. 2015, 14, 428–435. [CrossRef]
76. Charron, C.S.; Dawson, H.D.; Albaugh, G.P.; Solverson, P.M.; Vinyard, B.T.; Solano-Aguilar, G.I.; Molokin, A.; Novotny, J.A. A single meal containing raw, crushed garlic influences expression of immunity-and cancer-related genes in whole blood of humans. J. Nutr. 2015, 145, 2448–2455. [CrossRef]
77. Smith, S.C.; Collins, A.; Ferrari, R.; Holmes, D.R.; Logstrup, S.; McGhie, D.V.; Ralston, J.; Sacco, R.L.; Stam, H.; Taubert, K.; et al. Our time: A call to save preventable death from cardiovascular disease (heart disease and stroke). J. Am. Coll. Cardiol. 2012, 60, 2343–2348. [CrossRef] [PubMed]
78. Edirisinghe, I.; Banaszewski, K.; Cappozzo, J.; Sandhya, K.; Ellis, C.L.; Tadapaneni, R.; Kappagoda, C.T.; Burton-Freeman, B.M. Strawberry anthocyanin and its association with postprandial inflammation and insulin. Br. J. Nutr. 2011, 106, 913–922. [CrossRef]
79. Zhu, Y.; Anand, R.; Geng, X.; Ding, Y. A mini review: Garlic extract and vascular diseases. Neurol. Res. 2018, 40, 421–425. [CrossRef]
80. Siti, H.N.; Kamisah, Y.; Kamsiah, J. The role of oxidative stress, antioxidants and vascular inflammation in cardiovascular disease (a review). Vasc. Pharmacol. 2015, 71, 40–56. [CrossRef]
81. Leonarduzzi, G.; Gamba, P.; Gargiulo, S.; Biasi, F.; Poli, G. Inflammation-related gene expression by lipid oxidation-derived products in the progression of atherosclerosis. Free Radic. Biol. Med. 2012, 52, 19–34. [CrossRef]
82. Orekhov, A. Direct anti-atherosclerotic therapy; development of natural anti-atherosclerotic drugs preventing cellular cholesterol retention. Curr. Pharm. Des. 2013, 19, 5909–5928. [CrossRef]
83. Sobenin, I.A.; Pryanishnikov, V.V.; Kunnova, L.M.; Rabinovich, Y.A.; Martirosyan, D.M.; Orekhov, A.N. The e_ects of time-released garlic powder tablets on multifunctional cardiovascular risk in patients with coronary artery disease. Lipids Health Dis. 2010, 9, 119. [CrossRef] [PubMed]
84. Zeb, I.; Ahmadi, N.; Flores, F.; Budo_, M.J. Randomized trial evaluating the e_ect of aged garlic extract with supplements versus placebo on adipose tissue surrogates for coronary atherosclerosis progression. Coron. Artery Dis. 2018, 29, 325–328. [CrossRef]
85. Wlosinska, M.; Nilsson, A.C.; Hlebowicz, J.; Malmsjö, M.; Fakhro, M.; Lindstedt, S. Aged garlic extract preserves cutaneous microcirculation in patients with increased risk for cardiovascular diseases: A double-blinded placebo-controlled study. Int. Wound J. 2019, 16, 1487–1493. [CrossRef] [PubMed]
86. Myasoedova, V.A.; Kirichenko, T.V.; Melnichenko, A.A.; Orekhova, V.A.; Ravani, A.; Poggio, P.; Sobenin, I.A.; Bobryshev, Y.V.; Orekhov, A.N. Anti-atherosclerotic e_ects of a phytoestrogen-rich herbal preparation in postmenopausal women. Int. J Mol. Sci. 2016, 17, 1318. [CrossRef] [PubMed]
87. Matsumoto, S.; Nakanishi, R.; Li, D.; Alani, A.; Rezaeian, P.; Prabhu, S.; Abraham, J.; Fahmy, M.A.; Dailing, C.; Flores, F.; et al. Aged garlic extract reduces low attenuation plaque in coronary arteries of patients with metabolic syndrome in a prospective randomized double-blind study. J. Nutr. 2016, 146, 427S–432S. [CrossRef] [PubMed]
88. Sahebkar, A.; Serban, C.; Ursoniu, S.; Banach, M. E_ect of garlic on plasma lipoprotein (a) concentrations: A systematic review and meta-analysis of randomized controlled clinical trials. Nutrition 2016, 32, 33–40. [CrossRef]
89. Mahdavi-Roshan, M.; Mirmiran, P.; Arjmand, M.; Nasrollahzadeh, J. E_ects of garlic on brachial endothelial function and capacity of plasma to mediate cholesterol e_ux in patients with coronary artery disease. Anatol. J. Cardiol. 2017, 18, 116–121. [CrossRef] [PubMed]
90. Zeng, T.; Guo, F.F.; Zhang, C.L.; Song, F.Y.; Zhao, X.L.; Xie, K.Q. A meta-analysis of randomized, double-blind, placebo-controlled trials for the e_ects of garlic on serum lipid profiles. J. Sci. Food Agric. 2012, 92, 1892–1902. [CrossRef]
91. Shafiekhani, M.; Faridi, P.; Kojuri, J.; Namazi, S. Comparison of antiplatelet activity of garlic tablets with cardio-protective dose of aspirin in healthy volunteers: A randomized clinical trial. Avicenna J. Phytomed. 2016, 6, 550–557. [PubMed]
92. Wojcikowski, K.; Myers, S.; Brooks, L. E_ects of garlic oil on platelet aggregation: A double blind placebo controlled crossover study. Platelets 2007, 18, 29–34. [CrossRef]
93. Macan, H.; Uykimpang, R.; Alconcel, M.; Takasu, J.; Razon, R.; Amagase, H.; Niihara, Y. Aged garlic extract may be safe for patients on warfarin therapy. J. Nutr. 2006, 136, 793S–795S. [CrossRef] [PubMed]
94. Samson, S.L.; Garber, A.J. Metabolic syndrome. Endocrinol. Metab. Clinics. 2014, 43, 1–23. [CrossRef] [PubMed]
95. Choudhary, P.R.; Jani, R.D.; Sharma, M.S. E_ect of raw crushed garlic (Allium sativum L.) on components of metabolic syndrome. J. Diet. Suppl. 2018, 15, 499–506. [CrossRef]
96. Varma, M.; Sharma, D.K.; Paaneri, S.; Mishra, A.; Sinha, A.R.S.; Varma, V. Potential clinical benefits of garlic (Allium sativum). J. Environ. Res. Dev. 2011, 5, 652–655.
97. Gomez-Arbelaez, D.; Lahera, V.; Oubiña, P.; Valero-Muñoz, M.; Heras, N.D.L.; Rodríguez, Y.; Garcia, R.G.; Camacho, P.A.; López-Jaramillo, P. Aged garlic extract improves adiponectin levels in subjects with metabolic syndrome: A double-blind, placebo-controlled, randomized, crossover study. Mediat. Inflamm. 2013, 2013, 6. [CrossRef] [PubMed]
98. Magder, S. The meaning of blood pressure. Crit. Care 2018, 22, 257. [CrossRef] [PubMed]
99. Ried, K. Garlic lowers blood pressure in hypertensive individuals, regulates serum cholesterol, and stimulates immunity: An updated meta-analysis and review. J. Nutr. 2016, 146, 389S–396S. [CrossRef] [PubMed]
100. Ried, K.; Frank, O.R.; Stocks, N.P. Aged garlic extract reduces blood pressure in hypertensives: A dose–response trial. Eur. J. Clin. Nutr. 2013, 67, 64–70. [CrossRef] [PubMed]
101. Steiner, M.; Khan, A.H.; Holbert, D.; Lin, R.I. A double-blind crossover study in moderately hypercholesterolemic men that compared the e_ect of aged garlic extract and placebo administration on blood lipids. Am. J. Clin. Nutr. 1996, 64, 866–870. [CrossRef]
102. Ackermann, R.T.; Mulrow, C.D.; Ramirez, G.; Gardner, C.D.; Morbidoni, L.; Lawrence, V.A. Garlic shows promise for improving some cardiovascular risk factors. Arch. Intern. Med. 2001, 161, 813–824. [CrossRef] [PubMed]
103. Nakasone, Y.; Nakamura, Y.; Yamamoto, T.; Yamaguchi, H. E_ect of a traditional Japanese garlic preparation on blood pressure in prehypertensive and mildly hypertensive adults. Exp. Ther. Med. 2013, 5, 399–405. [CrossRef] [PubMed]
104. Zeb, F.; Safdar, M.; Fatima, S.; Khan, S.; Alam, S.; Muhammad, M.; Syed, A.; Habib, F.; Shakoor, H. Supplementation of garlic and coriander seed powder: Impact on body mass index, lipid profile and blood pressure of hyperlipidemic patients. Pak. J. Pharm. Sci. 2018, 31, 1935–1941. [PubMed]
105. Simons, L.A.; Balasubramaniam, S.; Von Konigsmark, M.; Parfitt, A.; Simons, J.; Peters,W. On the e_ect of garlic on plasma lipids and lipoproteins in mild hypercholesterolaemia. Atherosclerosis 1995, 113, 219–225. [CrossRef]
106. Sujithra, K.; Srinivasan, S.; Indumathi, D.; Vinothkumar, V. Allyl methyl sulfide, a garlic active component mitigates hyperglycemia by restoration of circulatory antioxidant status and attenuating glycoprotein components in streptozotocin-induced experimental rats. Toxicol. Mech. Methods 2019, 29, 165–176. [CrossRef] [PubMed]
107. Zheng, Y.; Ley, S.H.; Hu, F.B. Global aetiology and epidemiology of type 2 diabetes mellitus and its complications. Nat. Rev. Endocrinol. 2018, 14, 88–98. [CrossRef] [PubMed]
108. Herman, W.H. The global burden of diabetes: An overview. In Diabetes Mellitus in Developing Countries and Underserved Communities; Springer: Cham, Germany, 2017; pp. 1–5.
109. Melino, S.; Leo, S.; Toska Papajani, V. Natural Hydrogen Sulfide Donors from Allium sp. as a Nutraceutical Approach in Type 2 Diabetes Prevention and Therapy. Nutrition 2019, 11, 1581. [CrossRef] [PubMed]
110. Shabani, E.; Sayemiri, K.; Mohammadpour, M. The e_ect of garlic on lipid profile and glucose parameters in diabetic patients: A systematic review and meta-analysis. Prim. Care Diabetes 2019, 13, 28–42. [CrossRef]
111. Hou, L.Q.; Liu, Y.H.; Zhang, Y.Y. Garlic intake lowers fasting blood glucose: Meta-analysis of randomized controlled trials. Asia Pac. J. Clin. Nutr. 2015, 24, 575–582.
112. Phil, R.A.; Khan, R.A.; Ashraf, I. E_ects of garlic on blood glucose levels and HbA1c in patients with type 2 diabetes mellitus. J. Med. Plant Res. 2011, 5, 2922–2928.
113. Ghorbani, A.; Zarvandi, M.; Rakhshandeh, H. A Randomized Controlled Trial of a Herbal Compound for Improving Metabolic Parameters in Diabetic Patients with Uncontrolled Dyslipidemia. Endocr. Metab. Immune Disord. Drug Targets 2019, 19, 1075–1082. [CrossRef]
114. Ashraf, R.; Khan, R.A.; Ashraf, I. Garlic (Allium sativum) supplementation with standard antidiabetic agent provides better diabetic control in type 2 diabetes patients. Pak. J. Pharm. Sci. 2011, 24, 565–570.
115. Parham, M.; Bagherzadeh, M.; Asghari, M.; Akbari, H.; Hosseini, Z.; Rafiee, M.; Vafaeimanesh, J. Evaluating the e_ect of a herb on the control of blood glucose and insulin-resistance in patients with advanced type 2 diabetes (a double-blind clinical trial). Caspian J. Intern. Med. 2020, 11, 12–20. [PubMed]
116. Dehghani, S.; Alipoor, E.; Salimzadeh, A.; Yaseri, M.; Hosseini, M.; Feinle-Bisset, C.; Hosseinzadeh-Attar, M.J. The e_ect of a garlic supplement on the pro-inflammatory adipocytokines, resistin and tumor necrosis factor-alpha, and on pain severity, in overweight or obese women with knee osteoarthritis. Phytomedicine 2018, 48, 70–75. [CrossRef] [PubMed]
117. Salimzadeh, A.; Alipoor, E.; Dehghani, S.; Yaseri, M.; Hosseini, M.; Feinle-Bisset, C.; Hosseinzadeh-Attar, M.J. The e_ect of 12-week garlic supplementation on symptom relief in overweight or obese women with knee osteoarthritis. Int. J. Clin. Pract. Suppl. 2018, 72, e13208. [CrossRef] [PubMed]
118. Moza_ari-Khosravi, H.; Hesabgar, H.A.S.; Owlia, M.B.; Hadinedoushan, H.; Barzegar, K.; Fllahzadeh, M.H. The e_ect of garlic tablet on pro-inflammatory cytokines in postmenopausal osteoporotic women: A randomized controlled clinical trial. J. Diet. Suppl. 2012, 9, 262–271. [CrossRef] [PubMed]
119. Feily, A.; Namazi, M.R.; Pazyar, N.; Saboktakin, M.; Saboktakin, M. Garlic extract as a novel addition to antikeloid armamentarium: An untested hypothesis. J. Altern. Complement. Med. 2009, 15, 1153–1154. [CrossRef]
120. Kenawy, S.; Mohammed, G.F.; Younes, S.; Elakhras, A.I. Evaluation of TNF-_ serum level in patients with recalcitrant multiple common warts, treated by lipid garlic extract. Dermatol. Ther. 2014, 27, 272–277. [CrossRef]
121. Bakhshi, M.; Taheri, J.B.; Basir Shabestari, S.; Tanik, A.; Pahlevan, R. Comparison of therapeutic e_ect of aqueous extract of garlic and nystatin mouthwash in denture stomatitis. Gerodontology 2012, 29, e680–e684. [CrossRef]
122. Kundakovi´c, T.; Milenkovi´c, M.; Zlatkovi´c, S.; Nikoli´c, V.; Nikoli´c, G.; Bini´c, I. Treatment of venous ulcers with the herbal-based ointment Herbadermal®: A prospective non-randomized pilot study. Res. Complementary Med. 2012, 19, 26–30. [CrossRef]
123. Ejaz, S.; Chekarova, I.; Cho, J.W.; Lee, S.Y.; Ashraf, S.; Lim, C.W. E_ect of aged garlic extract on wound healing: A new frontier in wound management. Drug Chem. Toxicol. 2009, 32, 191–203. [CrossRef] [PubMed]
124. Ranjani, M.; Rajan, S.; Brindha, P. Antioxidant and antibacterial potentials of Aloe vera juice extract against wound isolates. J. Pure Appl. Microbiol. 2010, 4, 733–739.
125. Johnson, S.M.; Horn, T.D. Intralesional immunotherapy for warts using a combination of skin test antigens: A safe and e_ective therapy. J. Drugs Dermatol. JDD 2004, 3, 263–265. [PubMed]
126. Kus, S.; Ergun, T.; Gun, D.; Akin, O. Intralesional tuberculin for treatment of refractory warts. J. Eur. Acad. Dermatol. Venereol. 2005, 19, 515–516. [CrossRef] [PubMed]
127. Horn, T.D.; Johnson, S.M.; Helm, R.M.; Roberson, P.K. Intralesional immunotherapy of warts with mumps, Candida, and Trichophyton skin test antigens: A single-blinded, randomized, and controlled trial. Arch. Dermatol. 2005, 141, 589–594. [CrossRef] [PubMed]
128. Gökalp, F. The inhibition e_ect of garlic-derived compounds on human immunodeficiency virus type 1 and saquinavir. J. Biochem. Mol. Toxicol. 2018, 32, e22215. [CrossRef]
129. Serrano Gruhlke, H.D.A.; Mariezcurrena-Berasain, M.A.; Castillo, A.D.C.G.; Carranza, B.V.; Pliego, A.B.; Rojas, M.T.; Anele, U.Y.; Salem, A.Z.M.; Rivas-Caceres, R.R. Antimicrobial resistance of three common molecularly identified pathogenic bacteria to Allium aqueous extracts. Microb. Pathog. 2020, 142, 104028. [CrossRef]
130. Gruhlke, M.C.H.; Portz, D.; Stitz, M.; Anwar, A.; Schneider, T.; Jacob, C.; Schlaich, N.L.; Slusarenko, A.J. Allicin disrupts the cell’s electrochemical potential and induces apoptosis in yeast. Free Radic. Biol. Med. 2010, 49, 1916–1924. [CrossRef]
131. Said, M.M.;Watson, C.; Grando, D. Garlic alters the expression of putative virulence factor genes SIR2 and ECE1 in vulvovaginal C. albicans isolates. Sci. Rep. 2020, 10, 1–9. [CrossRef]
132. Gao, X.; Chen, Y.; Chen, Z.; Xue, Z.; Jia, Y.; Guo, Q.; Ma, Q.; Zhang, M.; Chen, H. Identification and antimicrobial activity evaluation of three peptides from laba garlic and the related mechanism. Food Funct. 2019, 10, 4486–4496. [CrossRef]
133. Thomas, A.; Thakur, S.; Habib, R. Comparison of antimicrobial e_cacy of green tea, garlic with lime, and sodium fluoride mouth rinses against Streptococcus mutans, Lactobacilli species, and Candida albicans in children: A randomized double-blind controlled clinical trial. Int. J. Clin. Pediatr. Dent. 2017, 10, 234–239. [PubMed]
134. Ebrahimy, F.; Dolatian, M.; Moatar, F.; Majd, H.A. Comparison of the therapeutic e_ects of Garcin® and fluconazole on Candida vaginitis. Singap. Med. J. 2015, 56, 567. [CrossRef] [PubMed]
135. Watson, C.J.; Grando, D.; Fairley, C.K.; Chondros, P.; Garland, S.M.; Myers, S.P.; Pirotta, M. The effects of oral garlic on vaginal candida colony counts: A randomised placebo controlled double-blind trial. BJOG 2014, 121, 498–506. [CrossRef]
136. Andrianova, I.V.; Sobenin, I.A.; Sereda, E.V.; Borodina, L.I.; Studenikin, M.I. E_ect of long-acting garlic tablets “allicor” on the incidence of acute respiratory viral infections in children. Ter. Arkhiv 2003, 75, 53–56.
137. Madineh, H.; Yadollahi, F.; Yadollahi, F.; Mofrad, E.P.; Kabiri, M. Impact of garlic tablets on nosocomial infections in hospitalized patients in intensive care units. Electron. Physician 2017, 9, 4064–4071. [CrossRef] [PubMed]
138. Foroutan-Rad, M.; Tappeh, K.H.; Khademvatan, S. Antileishmanial and Immunomodulatory Activity of Allium sativum (Garlic) A Review. J. Evid. Based Complement. Alternat. Med. 2017, 22, 141–155. [CrossRef]
139. Samdani, A.J.; Iqbal Choudhary, M. Laboratory studies and clinical trials on new formulations from garlic extract against cutaneous leishmaniasis. Anti-Infect. Agents 2012, 10, 111–116. [CrossRef]
140. Smyth, A.R.; Cifelli, P.M.; Ortori, C.A.; Righetti, K.; Lewis, S.; Erskine, P.; Holland, E.D.; Givskov, M.; Williams, P.; Cámara, M.; et al. Garlic as an inhibitor of Pseudomonas aeruginosa quorum sensing in cystic fibrosis—A pilot randomized controlled trial. Pediatr. Pulmonol. 2010, 45, 356–362.
141. Kim, H.N.; Kang, S.G.; Roh, Y.K.; Choi, M.K.; Song, S.W. E_cacy and safety of fermented garlic extract on hepatic function in adults with elevated serum gamma-glutamyl transpeptidase levels: A double-blind, randomized, placebo-controlled trial. Eur. J. Nutr. 2017, 56, 1993–2002. [CrossRef]
142. Panjeshahin, A.; Mollahosseini, M.; Panbehkar-Jouybari, M.; Kaviani, M.; Mirzavandi, F.; Hosseinzadeh, M. Effects of garlic supplementation on liver enzymes: A systematic review and meta-analysis of randomized controlled trials. Phytother. Res. 2020. [CrossRef]
143. Lee, M.H.; Kim, Y.M.; Kim, S.G. E_cacy and tolerability of diphenyl-dimethyl-dicarboxylate plus garlic oil in patients with chronic hepatitis. Int. J. Clin. Pharm. Ther. 2012, 50, 778–786. [CrossRef] [PubMed]
144. Soleimani, D.; Paknahad, Z.; Askari, G.; Iraj, B.; Feizi, A. E_ect of garlic powder consumption on body composition in patients with nonalcoholic fatty liver disease: Arandomized, double-blind, placebo-controlled trial. Adv. Biomed. Res. 2016, 5, 2. [CrossRef] [PubMed]
145. Zhang, S.; Gu, Y.;Wang, L.; Zhang, Q.; Liu, L.; Lu, M.; Meng, G.; Yao, Z.;Wu, H.; Xia, Y.; et al. Association between dietary raw garlic intake and newly diagnosed nonalcoholic fatty liver disease: A population-based study. Eur. J. Endocrinol. 2019, 181, 591–602. [CrossRef] [PubMed]
© 2020 by the authors. Licensee MDPI, Basel, Switzerland. This article is an open access article distributed under the terms and conditions of the Creative Commons Attribution (CC BY) license (http://creativecommons.org/licenses/by/4.0/).